题目内容
14.下列有关物质性质的描述中,正确的是( )| A. | Na2O的水溶液能导电,不能说明Na2O是电解质 | |
| B. | CO、NO、SO2都是大气污染物,在空气中都能稳定存在 | |
| C. | 石英和玛瑙的主要成分均为二氧化硅,其分子式为SiO2 | |
| D. | 酸性氧化物大多数是非金属氧化物,因此不能与酸溶液发生反应 |
分析 A.Na2O与水反应生成电解质;
B.一氧化氮与空气中的氧气反应生成二氧化氮;
C.二氧化硅为原子晶体,不存在分子;
D.二氧化硫为酸性氧化物,能够与硝酸发生氧化还原反应.
解答 解:A.Na2O与水反应生成电解质NaOH,所以Na2O的水溶液能导电,这不能说明Na2O是电解质,故A正确;
B.一氧化氮与空气中的氧气反应生成二氧化氮,在空气中不能稳定存在,故B错误;
C.二氧化硅为原子晶体,不存在分子,没有分子式,故C错误;
D.二氧化硫为酸性氧化物,能够与硝酸发生氧化还原反应,故D错误;
故选:A.
点评 本题考查了元素化合物知识,明确电解质、酸性氧化物的概念,熟悉一氧化氮、二氧化硫的性质是解题关键,注意只有分子晶体才存在分子式,题目难度不大.

练习册系列答案
相关题目
4.在水溶液中,下列电离方程式正确的是( )
| A. | CH3COOH═CH3COO-+H+ | B. | NaHSO4═Na++HSO4- | ||
| C. | HCO3-═H++CO32- | D. | HPO4-?H++PO43- |
5.在卤代烃R-CH2-CH2-X中,其化学键如图所示,当该卤代烃断键方式正确的是( )


| A. | 在氢氧化钠溶液中加热时,被破坏的键是①和③ | |
| B. | 在氢氧化钠乙醇溶液中加热时,被破坏的键是①和④ | |
| C. | 在氢氧化钠溶液中加热时,被破坏的键是① | |
| D. | 在氢氧化钠乙醇溶液中加热时,被破坏的键是①和② |
9.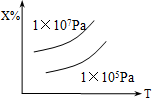 已知X(g)+2Y(g)?nZ的反应达到平衡状态时,体系中X的质量分数与温度(T),压强的关系如下图所示,下列说法中正确的是( )
已知X(g)+2Y(g)?nZ的反应达到平衡状态时,体系中X的质量分数与温度(T),压强的关系如下图所示,下列说法中正确的是( )
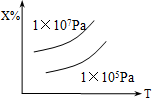 已知X(g)+2Y(g)?nZ的反应达到平衡状态时,体系中X的质量分数与温度(T),压强的关系如下图所示,下列说法中正确的是( )
已知X(g)+2Y(g)?nZ的反应达到平衡状态时,体系中X的质量分数与温度(T),压强的关系如下图所示,下列说法中正确的是( )| A. | Z是气态,n=3,正反应△H<0 | B. | Z是气态,n>3,正反应△H<0 | ||
| C. | Z是气态,n=3,正反应△H>0 | D. | Z不是气态,n<3,正反应△H>0 |
19.以下关于氟、氯、溴、碘的性质叙述错误的是( )
| A. | HF、HCl、HBr、HI稳定性逐渐减弱 | |
| B. | 单质F2、Cl2、Br2、I2中,与氢气化合最容易的是F2 | |
| C. | HF、HCl、HBr、HI中酸性最强的是HF | |
| D. | 单质F2、Cl2、Br2、I2中,I2的沸点最高 |
3.下列实验方案可行的是( )
| A. | 溴乙烷消去制取乙烯,产物性质的检验,直接将生成物通入溴的四氯化碳溶液,无需除杂 | |
| B. | 在淀粉溶液中加稀硫酸充分反应后,再加入银氨溶液,可检验淀粉的水解产物 | |
| C. | 除去苯中的苯酚,可加入NaOH溶液后再分液 | |
| D. | 将氯乙烷与NaOH的乙醇溶液共热,将产生的气体直接通入酸性高锰酸钾溶液中,溶液褪色,证明氯乙烷发生了消去反应 |
4.厨房中的物质放入足量的水中,充分搅拌,不能形成溶液的是( )
| A. | 食用油 | B. | 白醋 | C. | 白糖 | D. | 食盐 |
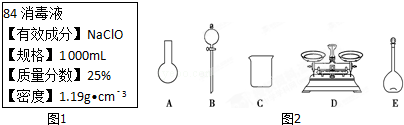

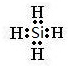 .
. .
.