题目内容
(16分)合成氨技术的发明使工业化人工固氮成为现实。
(1)已知N2(g)+3H2(g) 2NH3(g)
2NH3(g)  H=-92.2kJ·mol-1。在一定条件下反应时,当生成标准状况下33.6LNH3时,放出的热量为 。
H=-92.2kJ·mol-1。在一定条件下反应时,当生成标准状况下33.6LNH3时,放出的热量为 。
(2)合成氨混合体系在平衡状态时NH3的百分含量与温度的关系如下图所示。由图可知:

①温度T1、T2时的平衡常数分别为K1、K2,则K1 K2 (填“>”或“<”)。若在恒温、恒压条件下,向平衡体系中通入氦气,平衡 移动、(填“向左”、“向右”或“不”)。
②T2温度时,在1L的密闭容器中加入2.1mol N2、l.5molH2,经10min达到平衡,则v(H2)= 。达到平衡后,如果再向该容器内通入N2、H2、NH3各0.4mol,则平衡 移动(填“向左”、“向右”或“不”)。
(3)工业上用CO2和NH3反应生成尿素:CO2(g)+2NH3(g) H2O(1)+CO(NH2)2(1) △H,
H2O(1)+CO(NH2)2(1) △H,
在一定压强下测得如下数据:

①则该反应△H 0,表中数据a d,b f(均选填“>”、‘‘=”或“<”)。
②从尿素合成塔内出来的气体中仍含有一定量的CO2、NH3,应如何处理 。
(1)已知N2(g)+3H2(g)
 2NH3(g)
2NH3(g)  H=-92.2kJ·mol-1。在一定条件下反应时,当生成标准状况下33.6LNH3时,放出的热量为 。
H=-92.2kJ·mol-1。在一定条件下反应时,当生成标准状况下33.6LNH3时,放出的热量为 。(2)合成氨混合体系在平衡状态时NH3的百分含量与温度的关系如下图所示。由图可知:

①温度T1、T2时的平衡常数分别为K1、K2,则K1 K2 (填“>”或“<”)。若在恒温、恒压条件下,向平衡体系中通入氦气,平衡 移动、(填“向左”、“向右”或“不”)。
②T2温度时,在1L的密闭容器中加入2.1mol N2、l.5molH2,经10min达到平衡,则v(H2)= 。达到平衡后,如果再向该容器内通入N2、H2、NH3各0.4mol,则平衡 移动(填“向左”、“向右”或“不”)。
(3)工业上用CO2和NH3反应生成尿素:CO2(g)+2NH3(g)
 H2O(1)+CO(NH2)2(1) △H,
H2O(1)+CO(NH2)2(1) △H,在一定压强下测得如下数据:

①则该反应△H 0,表中数据a d,b f(均选填“>”、‘‘=”或“<”)。
②从尿素合成塔内出来的气体中仍含有一定量的CO2、NH3,应如何处理 。
(16分)
(1)69.15kJ(2分)
(2)① >(1分) 向左(1分) ②0.09 mol·L-1·min-1(2分) 向右(2分)
(3)①>(2分) < (2分) <(2分)
②净化后重新充入合成塔内,循环利用,提高原料利用率(2分)
(1)69.15kJ(2分)
(2)① >(1分) 向左(1分) ②0.09 mol·L-1·min-1(2分) 向右(2分)
(3)①>(2分) < (2分) <(2分)
②净化后重新充入合成塔内,循环利用,提高原料利用率(2分)
试题分析:(1)标准状况下33.6LNH3物质的量为:33.6L÷22.4L/mol=1.5mol,92.2kJ·mol-1÷2×1.5mol=69.15kJ。
(2)①根据图像,B点NH3的百分含量小于A点NH3的百分含量,所以K1 > K2;若在恒温、恒压条件下,向平衡体系中通入氦气,原反应体系气体的压强减小,平衡向气体系数增大的方向移动,即向左移动。
②根据“三段式”进行计算,设N2转化浓度为X,则
N2(g)+3H2(g)
 2NH3(g)
2NH3(g)起始浓度(mol?L?1) 2.1 1.5 0
转化浓度(mol?L?1) X 3X 2X
平衡浓度(mol?L?1)2.1—X 1.5—3X 2X
根据T1时NH3的百分含量为20%,则2X/(2.1—X+1.5—3X+2X)=20%,解得X=0.3,则v(H2)=0.9mol/L÷10min="0.09" mol·L-1·min-1;根据平衡浓度可求平衡常数K=(0.6mol?L?1)2÷[1.8mol/L×(0.6mol?L?1)3]=0.93(mol?L?1)-2,再向该容器内通入N2、H2、NH3各0.4mol,则Q=(1mol?L?1)2÷[2.2mol/L×(1mol?L?1)3]=0.45(mol?L?1)-2,Q < K,所以平衡向右移动。
(3)①根据表中数据,温度升高,CO2的转化率增大,平衡向右移动,所以正反应为吸热反应,?H > 0;n(NH3)/n(CO2)增大,CO2的转化率增大,所以a < d,b <f。
②CO2、NH3为反应物,所以净化后重新充入合成塔内,循环利用,提高原料利用率。

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
 Y(g)+Z(g) △H<0,反应到8min时达到平衡;在14min时改变体系的温度, 16min时建立新平衡。X的物质的量浓度变化如图所示。下列有关说法正确的是
Y(g)+Z(g) △H<0,反应到8min时达到平衡;在14min时改变体系的温度, 16min时建立新平衡。X的物质的量浓度变化如图所示。下列有关说法正确的是
 为放热反应,一定温度下在密闭容器中进行反应,
为放热反应,一定温度下在密闭容器中进行反应,

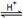 HCOOH(l) + CH3OH(l),反应吸热,但焓变的值很小。常温常压下,水解反应速率和平衡常数都较小。
HCOOH(l) + CH3OH(l),反应吸热,但焓变的值很小。常温常压下,水解反应速率和平衡常数都较小。
 XC(g),经 2 s后反应达平衡,测得 C 的浓度为 0.6 mol·L-1 ,B的物质的量为1.4 mol,现有下列几种说法:
XC(g),经 2 s后反应达平衡,测得 C 的浓度为 0.6 mol·L-1 ,B的物质的量为1.4 mol,现有下列几种说法:  AB来说,常温下按以下情况进行反应:
AB来说,常温下按以下情况进行反应: