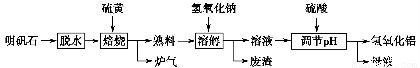
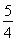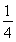题目内容
某化学兴趣小组的同学利用下图所示实验装置进行某些气体的制备、性质等实验(图中夹持装置有省略)。请按要求填空:
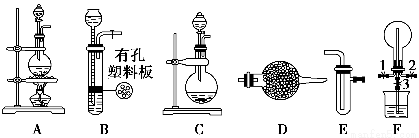
Ⅰ.探究氯气与氨气的反应
(1)为制取干燥氨气,可将装置C与________(填装置编号)连接;装置C中的烧瓶内固体宜选用________。
a.碱石灰 b.氯化钙 c.五氧化二磷 d.生石灰
(2)装置A、E、E连接可制取纯净、干燥的氯气,则两个E装置内的药品依次是________________。
(3)装置F可用于探究氯气与氨气(已知氯气与氨气可发生反应:3Cl2+2NH3=N2+6HCl)的反应。实验时打开弹簧夹1、3,关闭2,先向烧瓶中通入________,然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的另一种气体。实验一段时间后烧瓶内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体中的阳离子__________________________________________________________。
Ⅱ.探究某些物质的性质
(4)利用装置A、E,可设计实验比较Cl-和Br-的还原性强弱,能证明结论的实验现象是_______________________________________________________。
(5)若利用装置A、E进行乙烯与溴水反应的实验,写出反应的化学方程式_________________________________________________________________。
(6)将装置B、C分别与F相连后,进行H2S与SO2反应的实验。F的烧瓶中发生反应的化学方程式为______________________;F的烧杯所起的作用是_________________________________________________________________。
(1)D ad
(2)饱和食盐水、浓硫酸
(3)氯气 取少量固体于试管中,加入适量浓NaOH溶液并加热,在管口用湿润的红色石蕊试纸检验产生的气体,若湿润的红色石蕊试纸变蓝,[或用蘸有浓盐酸(或浓硝酸)的玻璃棒放在试管口,若有白烟生成],证明固体中有NH4+
(4)装置E中的NaBr溶液变橙红色
(5)CH2=CH2+Br2―→Br—CH2—CH2—Br
(6)SO2+2H2S=3S↓+2H2O 吸收尾气
【解析】(1)制取NH3,可用浓氨水的分解制备,然后再用碱石灰或生石灰干燥,但不能用CaCl2,因为CaCl2可结合NH3生成CaCl2·8NH3。(2)制取干燥纯净的Cl2,可用饱和食盐水除HCl,再用浓H2SO4干燥Cl2。(3)应向烧瓶中先通Cl2,再通NH3,因为Cl2有颜色,便于观察;一开始若通NH3,由于弹簧夹3打开,容易形成喷泉。证明NH要注意“操作→现象→结论”,同时还要注意细节,如浓NaOH,加热,湿润等。(4)可利用Cl2+2NaBr=2NaCl+Br2,证明还原性Br->Cl-。(5)CH2=CH2+Br2―→CH2BrCH2Br。(6)SO2+2H2S=3S↓+2H2O;F可用来吸收剩余的SO2或H2S。