题目内容
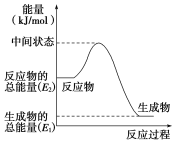
【题目】已知热化学方程式:2SO2(g)+O2(g) ![]() 2SO3(g)ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是
2SO3(g)ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是
A.相同条件下,2 mol SO2(g)和1 mol O2(g)所具有的能量小于2 mol SO3(g)所具有的能量
B.2 mol SO2(g)和1 mol O2(g)在密闭容器中充分反应,放出热量小于Q kJ
C.增大压强或升高温度,该反应过程都能放出更多的热量
D.2 mol SO2(g)和1 mol O2(g)在密闭容器中充分反应,放出热量等于Q kJ
【答案】B
【解析】
试题分析:A.由题意知该反应是放热反应,相同条件下,2molSO2(g)和1molO2(g)所具有的能量大于2molSO3(g)所具有的能量,故A错误;B.将2molSO2(g)和1molO2(g)置于一密闭容器中充分反应后,达到化学平衡,反应物不能全部转化,放出热量小于QkJ,故B正确;C.反应是气体体积减小的放热反应,增大压强平衡正向进行,升高温度,该平衡向逆反应方向移动,故C错误;D.将2molSO2(g)和1molO2(g)置于一密闭容器中充分反应后,达到化学平衡,反应物不能全部转化,放出热量小于QkJ,故D错误。故选B。

【题目】下表是元素周期表一部分,列出了十个元素在周期表中的位置:
族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ⑥ | |||||||
3 | ① | ③ | ⑤ | ⑦ | ⑧ | ⑩ | ||
4 | ② | ④ | ⑨ |
请用化学用语回答下列问题
(1)在①~⑦元素中,原子半径最大的是 (填元素符号);
(2)①~⑩中元素最高价氧化物对应的水化物中酸性最强的是 (填物质化学式),⑤所对应元素的单质工业制备方法为 。
(3)用电子式表示元素③与⑧形成化合物的过程 。
(4)我国首创以单质⑤—空气—海水电池作为能源的新型的海水标志灯,以海水为电解质溶液,靠空气中的氧气使单质⑤不断氧化而产生电流,只要把灯放入海水数分钟,就会发出耀眼的白光。则电源的负极反应是 ,正极反应为 。