题目内容
13.2.2g某化合物中含有3.01×1022个甲分子,则甲的摩尔质量为( )| A. | 44g/mol | B. | 2.2mol | C. | 44g | D. | 22 |
分析 根据n=$\frac{N}{{N}_{A}}$、M=$\frac{m}{M}$ 来计算甲的摩尔质量,然后选择正确答案即可.
解答 解:2.2g某化合物中含有3.01×1022个甲分子,
则n=$\frac{3.01×1{0}^{22}}{6.02×1{0}^{23}}$=0.05mol,
所以M=$\frac{2.2g}{0.05mol}$=44g/mol,故选A.
点评 本题考查物质的量的有关计算,熟悉以物质的量为中心的计算及计算公式即可解答,难度不大.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案
相关题目
3.根据电离平衡原理,设计实验证明NH3•H2O是弱碱.
可选用的试剂:酚酞、石蕊、稀氨水、醋酸铵晶体和蒸馏水.
可选用的试剂:酚酞、石蕊、稀氨水、醋酸铵晶体和蒸馏水.
| 实验操作 | 实验现象 |
| ①取少量氨水于试管中,滴加酚酞试液 ②向试管中加入少量醋酸铵晶体,振荡 | 溶液呈红色 红色变浅 |
| 结论:氨水中存在电离平衡,证明氨水是弱碱 | |
4.对于X+Y(s)?Z的平衡,若增大压强,Y的转化率增大,则X和Y的状态是( )
| A. | X为气态,Z为固态 | B. | X为固态,Z为气态 | C. | X为气态,Z为气态 | D. | X为固态,Z为固态 |
1.下列物质属于非电解质的是( )
| A. | 金属钠 | B. | CH3COOH | C. | H2SO4 | D. | SO2 |
5.当光速通过下列分散系:①豆浆 ②混有尘埃的空气 ③稀盐酸 ④蒸馏水 能观察到有丁达尔效应的是( )
| A. | ①③ | B. | ②④ | C. | ①② | D. | ①④ |
2.某烃含碳、氢元素的质量比为6:l,对氮气的相对密度为2,该烃既可使溴水褪色,又能与氢气加成,与氢气加成的产物的二氯化物有3种同分异构体,则该烃为( )
| A. | CH2═CH2 | B. | CH2═CH-CH2CH3 | C. | 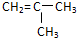 | D. | CH2═CH-CH═CH2 |
3.“绿色奥运”是2008北京奥运会的主题之一.为减轻污染,北京市为汽车加装了“三元催化净化器”,可将尾气中的CO、NO转化为参与大气循环的无毒混合气体,该混合气体是( )
| A. | CO2和N2 | B. | CO2和NO2 | C. | CO2和O2 | D. | CO2、N2和O2 |