题目内容
已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
| 温度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
830℃时,向一个2 L的密闭容器中充入0.2mol的A和0.8mol的B,反应初始4 s内A的平均反应速率v(A)=0.005 mol/(L·s)。下列说法正确的是
A.4 s时c(B)为0.76 mol/L
B.830℃达平衡时,A的转化率为80%
C.反应达平衡后,升高温度,平衡正向移动
D.1200℃时反应C(g)+D(g)
 A(g)+B(g)的平衡常数的值为0.4
A(g)+B(g)的平衡常数的值为0.4
B
解析试题分析:A.由于反应初始4 s内A的平均反应速率v(A)="0.005" mol/(L·s),V(B)="V(A)=" 0.005 mol/(L·s),所以4 s时c(B)为(0.8mol ÷2L)-0.005 mol/(L·s)×4s="0.36" mol/L.错误。B.830℃化学平衡常数为1.0.当反应达平衡时,假设c(A)=x,根据化学平衡常数 ,解得x=0.08.所以A的转化率为(0.08÷0.1)×100%=80%.正确。C.根据表格的数据可以看出:温度升高,化学平衡常数减小。说明升高温度,化学平衡逆向移动。根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动。逆反应方向为吸热反应。错误。D.1200℃时A(g)+B(g)
,解得x=0.08.所以A的转化率为(0.08÷0.1)×100%=80%.正确。C.根据表格的数据可以看出:温度升高,化学平衡常数减小。说明升高温度,化学平衡逆向移动。根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动。逆反应方向为吸热反应。错误。D.1200℃时A(g)+B(g) C(g)+D(g)的平衡常数
C(g)+D(g)的平衡常数 而反应C(g)+D(g)
而反应C(g)+D(g) A(g)+B(g)的平衡常数
A(g)+B(g)的平衡常数 。
。
考点:考查化学平衡常数与温度、浓度计反应的正、逆性的关系的知识。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案在673K、30MPa下,在密闭容器中进行合成氨反应: N2(g)+3H2(g) 2NH3(g) △H<0,n(NH3)和n(H2)随时间(t)的变化关系如右图所示。下列分析一定正确的是
2NH3(g) △H<0,n(NH3)和n(H2)随时间(t)的变化关系如右图所示。下列分析一定正确的是
| A.正反应速率:a点小于b点 |
| B.c点处反应达到平衡 |
| C.d点和e点处的n(N2)不一样 |
| D.若其他条件不变,在773 K时反应至t1时刻,n(H2)比图中d点对应的n(H2)大 |
CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示。下列结论不正确的是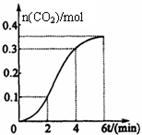
| A.反应开始2分钟内平均反应速率最大 |
| B.反应4分钟后平均反应速率最小 |
| C.反应开始4分钟内温度对反应速率的影响比浓度大 |
| D.反应4分钟后反应速率下降的原因是盐酸浓度逐渐减小 |
将等物质的量的N2、H2气体充入某密闭容器中,在一定条件下,发生如下反应并达到平衡:N2(g)+3H2 (g) 2NH3 (g);△H<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是
2NH3 (g);△H<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是
| | 改变条件 | 新平衡与原平衡比较 |
| A | 增大压强 | N2的浓度一定变小 |
| B | 升高温度 | N2的转化率变小 |
| C | 充入一定量H2 | H2的转化率不变,N2的转化率变大 |
| D | 使用适当催化剂 | NH3的体积分数增大 |
已知反应2CO(g)=2C(s)+O2(g)的△H为正值,△S为负值。设△H和△S不随温度而变,下列说法正确的是
| A.低温下能自发进行 |
| B.高温下能自发进行 |
| C.低温下不能自发进行,高温下能自发进行 |
| D.任何温度下都不能自发进行 |
反应C(s)+H2O(g) CO(g)+ H2(g)在一容积可变的密闭容器中进行。下列条件的改变对其反应速率几乎无影响的是
CO(g)+ H2(g)在一容积可变的密闭容器中进行。下列条件的改变对其反应速率几乎无影响的是
| A.压缩容器体积,增大体系压强 |
| B.加入适当的催化剂 |
| C.保持压强不变,充入惰性气体使容器容积增大 |
| D.保持容器容积不变,充入惰性气体使体系压强增大 |
一定条件下,可逆反应2X(g)+3Y(g) 4Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.2mol·L-1、0.3 mol·L-1、0.16 mol·L-1,则下列判断不合理的是
4Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.2mol·L-1、0.3 mol·L-1、0.16 mol·L-1,则下列判断不合理的是
| A.c1∶c2=2∶3 |
| B.X、Y的转化率不相等 |
| C.平衡时,Y和Z的生成速率之比为3∶4 |
| D.c1的取值范围为0<c1<0.28 mol·L-1 |
 2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法: 2Z(g);ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是( )
2Z(g);ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是( )