题目内容
【题目】设NA为阿伏加德罗常数的值,则下列说法正确的是
A. 标准状况下,2.24 LCCl4中含Cl原子数目为0.4NA
B. 28g聚乙烯中所含原子数为6NA
C. 0.1mol苯乙烯中含有双键的数目为0.4NA
D. 15g甲基(—CH3)中含有电子的数目为10NA
【答案】B
【解析】分析:A.标准状况下四氯化碳是液体;
B.根据聚乙烯的物质的量和分子式判断;
C.苯环中不含有碳碳双键;
D.甲基含有9个电子。
详解A. 标准状况下四氯化碳是液体,不能利用气体摩尔体积计算2.24 LCCl4中含Cl原子数目为,A错误;
B. 28g聚乙烯中所含原子的物质的量是![]() ,原子数为6NA,B正确;
,原子数为6NA,B正确;
C. 苯环中不含有碳碳双键,0.1mol苯乙烯中含有双键的数目为0.1NA,C错误;
D. 15g甲基(-CH3)的物质的量是1mol,其中含有电子的数目为9NA,D错误。答案选B。

练习册系列答案
相关题目
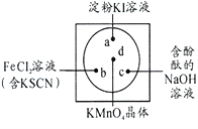
【题目】下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。已知:2KMnO4+16HCl―→2KCl+5Cl2↑+2MnCl2+8H2O

对实验现象的“解释或结论”正确的是 ( )
选项 | 实验现象 | 解释或结论 |
A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
C | d处立即褪色 | 氯气与水生成了漂白性物质 |
D | e处变红色 | 还原性:Fe2+>Cl- |
A. A B. B C. C D. D