题目内容
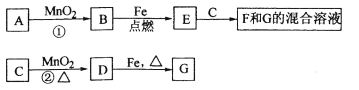
【题目】晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:①高温下用碳还原二氧化硅制得粗硅;②粗硅与Cl2加热反应制得四氯化硅;③四氯化硅经精馏提纯后与过量H2在高温下反应制得高纯硅。请依次写出所涉及的反应方程式:
①___________________________________________;
②____________________________________________;
③_____________________________________________;
【答案】2C +SiO2![]() Si+2CO Si +2Cl2
Si+2CO Si +2Cl2![]() SiCl4 SiCl4+2H2
SiCl4 SiCl4+2H2![]() Si+4HCl
Si+4HCl
【解析】
①高温下用碳还原二氧化硅制得粗硅,反应方程式为:2C +SiO2![]() Si+2CO;
Si+2CO;
②粗硅与Cl2加热反应制得四氯化硅,反应方程式为:Si +2Cl2![]() SiCl4;
SiCl4;
③四氯化硅经精馏提纯后与过量H2在高温下反应制得高纯硅,反应方程式为:SiCl4+2H2![]() Si+4HCl;
Si+4HCl;
①高温下用碳还原二氧化硅制得粗硅,反应方程式为:2C +SiO2![]() Si+2CO;故答案为:2C +SiO2
Si+2CO;故答案为:2C +SiO2![]() Si+2CO;
Si+2CO;
②粗硅与Cl2加热反应制得四氯化硅,反应方程式为:Si +2Cl2![]() SiCl4;故答案为:Si +2Cl2
SiCl4;故答案为:Si +2Cl2![]() SiCl4;
SiCl4;
③四氯化硅经精馏提纯后与过量H2在高温下反应制得高纯硅,反应方程式为:SiCl4+2H2![]() Si+4HCl;故答案为:SiCl4+2H2
Si+4HCl;故答案为:SiCl4+2H2![]() Si+4HCl;
Si+4HCl;

 阅读快车系列答案
阅读快车系列答案【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
a | |||||||||||||||||
b | c | d | e | f | |||||||||||||
g | h | i | j | k | l | m | |||||||||||
n | o | ||||||||||||||||
试回答下列问题:
(1)请写出元素o的基态原子电子排布式________
(2)d的最简单氢化物的分子空间立体构型为_________,中心原子的杂化形式为_________;k在空气中燃烧产物的分子空间立体构型为________,中心原子的杂化形式为______,该分子是_____(填“极性”或“非极性”)分子。
(3)第三周期8种元素按单质熔点高低的顺序如下图,其中序号“8”代表______(填元素符号);其中电负性最大的是_______(填下图中的序号)。
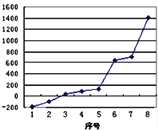
(4)由j原子跟c原子以1 : 1相互交替结合而形成的晶体,晶型与晶体j相同。两者相比 熔点更高的是________(填化学式),试从结构角度加以解释:______________________________