题目内容
【题目】通常人们把拆开1mol某化学键所消耗的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热.
化学键 | Si﹣O | Si﹣Cl | H﹣H | H﹣Cl | Si﹣Si | Si﹣C |
E(kJmol﹣1) | 460 | 360 | 436 | 431 | 176 | 347 |
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g) ![]() Si(s)+4HCl(g),(已知1mol晶体Si中有2molSi﹣Si键),该反应的产生的热量为( )
Si(s)+4HCl(g),(已知1mol晶体Si中有2molSi﹣Si键),该反应的产生的热量为( )
A.吸收412 kJmol﹣1
B.放出412 kJmol﹣1
C.吸收236 kJmol﹣1
D.放出236 kJmol﹣1
【答案】C
【解析】解:工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g) ![]() Si(s)+4HCl(g),反应热=反应物的键能之和﹣生成物的键能之和,即△H=360kJ/mol×4+436kJ/mol×2﹣176kJ/mol×2﹣431kJ/mol×4=+236 kJ/mol,△H>0,该正反应为吸热,
Si(s)+4HCl(g),反应热=反应物的键能之和﹣生成物的键能之和,即△H=360kJ/mol×4+436kJ/mol×2﹣176kJ/mol×2﹣431kJ/mol×4=+236 kJ/mol,△H>0,该正反应为吸热,
故选C.

【题目】某学习小组通过下列装置探究MnO2与FeCl3·6H2O能否反应产生Cl2。

实验操作和现象:
操作 | 现象 |
点燃酒精灯,加热 | ⅰ.A中部分固体溶解,上方出现白雾 ⅱ.稍后,产生黄色气体,管壁附着黄色液滴 ⅲ.B中溶液变蓝 |
(1)现象ⅰ中的白雾是________,FeCl3·6H2O形成白雾的原因是_________(用化学方程式表示)
(2)分析现象ⅰ和ⅱ,推测黄色气体的成分,有以下三种可能:
甲.氯气 乙.氯化铁 丙.既有氯气又有氯化铁
①为检验黄色气体中是否存在氯化铁,应将黄色气体通入______溶液,出现_____(描述现象), 黄色气体中存在氯化铁说明氯化铁具有的性质为__________。结论: 乙或丙成立。
②为进一步确认乙还是丙正确,尚需证明氯气是否存在
方法一:直接检验,检验试剂为_________。
方法二:先除去氯化铁,除杂试剂为___________;再用淀粉碘化钾溶液检验氯气。
(3)实验证明,丙成立。另外,将A中产物分离得到Fe2O3和MnCl2,则A中发生反应的化学方程式是____。
【题目】(1)为了减轻汽车尾气造成的大气污染,人们开始探索利用NO和CO在一定条件下 转化为两种无毒气体E和F的方法(已知该反应△H<0). 在2 L密闭容器中加入一定量NO和CO,当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
| NO | CO | E | F |
初始 | 0.100 | 0.100 | 0 | 0 |
T1 | 0.020 | 0.020 | 0.080 | 0.040 |
T2 | 0.010 | 0.010 | 0.090 | 0.045 |
① 请结合上表数据,写出NO与CO反应的化学方程式________________________。
② 根据表中数据判断,温度T1和T2的关系是(填序号)_________________________。
A.T1>T2 B.T1<T2 C.T1=T2 D.无法比较
(2)已知:4NH3(g) + 3O2(g) = 2N2(g) + 6H2O(g) ΔH= - 1266.8 kJ/mol,N2(g) + O2(g) = 2NO(g) ΔH = + 180.5kJ/mol,则氨催化氧化的热化学方程式为_________________。
(3)500℃下,在A、B两个容器中均发生合成氨的反应。隔板Ⅰ固定不动,活塞Ⅱ可自由移动。
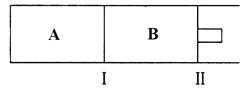
当合成氨在容器B中达平衡时,测得其中含有1.0molN2,0.4molH2,0.4molNH3,此时容积为2.0L。则此条件下的平衡常数为_______________;保持温度和压强不变,向此容器中通入0.36molN2,平衡将_______________(填“正向”、“逆向”或“不”)移动。