题目内容
19.所含化学键与NaOH完全相同的物质是( )| A. | NaCl | B. | MgCl2 | C. | K2SO4 | D. | NH3 |
分析 NaOH中钠离子与氢氧根离子之间形成离子键,O与H之间形成共价键,由此分析解答.
解答 解:A、NaCl中钠离子与氯离子是以离子键结合,故A不符合;
B、MgCl2中镁离子与氯离子是以离子键结合,故B不符合;
C、K2SO4中有离子键和共价键,故C符合;
D、NH3中只存在共价键,故D不符合;
故选C.
点评 本题考查化学键的判断,把握化学键的形成及判断的一般规律为解答的关键,注意特殊物质中的化学键,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
10.下列关于有机物的说法正确的是( )
| A. | 纯净物C4H8的核磁共振氢谱峰最多为4 | |
| B. | 化学式为C8H8的有机物,一定能使酸性高锰酸钾溶液褪色 | |
| C. |  的同分异构体中,可以有醇、酚类物质 的同分异构体中,可以有醇、酚类物质 | |
| D. | 1 mol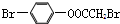 最多能与2 mol NaOH反应 最多能与2 mol NaOH反应 |
7.下列关于苯的叙述正确的是( )


| A. | 反应①为取代反应,有机产物的密度比水小 | |
| B. | 反应②为氧化反应,反应现象是火焰明亮并带有较多的黑烟 | |
| C. | 反应③为取代反应,有机产物是一种烃 | |
| D. | 反应④1mol苯最多与3molH2发生加成反应,是因为苯分子含有三个碳酸双键 |
14.对于放射性同位素${\;}_{53}^{133}$I,其左下角数字“53”表示( )
| A. | 质量数 | B. | 中子数 | C. | 质子数 | D. | 电子数 |
4.工业上生产硫酸时,利用催化氧化反应将二氧化硫转化为三氧化硫是一个关键步骤,在密闭容器中压强及温度对SO2转化率(利用率)的影响如表:
(1)写出二氧化硫转化为三氧化硫的化学方程式2SO2+O2?2SO3. 根据表中数据可知,生成 SO3 的反应属于放热反应(填“放热”或“吸热”. )
(2)在其他条件不变的情况下,扩大容器体积以减小反应体系的压强,v正减小 (填“增大”或“减小”,下同),v逆减小,平衡向逆反应方向移动(选填“正反应”或“逆反应”).
(3)若容器容积为2L,开始加入SO2为0.20mol,10s后测得SO2 的物质的量为0.16mol,则O2的平均反应速率为0.001mol(L•S);若即系通入氧气,则平衡时的SO2转化率增大(选填“增大”或“减小”)
(4)在 400℃~500℃时,SO2 的催化氧化采用常压而不是高压,其主要原因是常压时的转化率较高、高压成本高.
| 转化率(%) | 0.1MPa | 0.5MPa | 1.0MPa | 10MPa |
| 400℃ | 99.2% | 99.6% | 99.7% | 99.9% |
| 500℃ | 93.5% | 96.9% | 97.8% | 99.3% |
| 600℃ | 73.7% | 85.8% | 89.5% | 96.4% |
(2)在其他条件不变的情况下,扩大容器体积以减小反应体系的压强,v正减小 (填“增大”或“减小”,下同),v逆减小,平衡向逆反应方向移动(选填“正反应”或“逆反应”).
(3)若容器容积为2L,开始加入SO2为0.20mol,10s后测得SO2 的物质的量为0.16mol,则O2的平均反应速率为0.001mol(L•S);若即系通入氧气,则平衡时的SO2转化率增大(选填“增大”或“减小”)
(4)在 400℃~500℃时,SO2 的催化氧化采用常压而不是高压,其主要原因是常压时的转化率较高、高压成本高.
11.下列说法正确的是( )
| A. | 蛋白质、纤维、油脂、淀粉、聚乙烯都是高分子化合物 | |
| B. | 蛋白质的水解产物为氨基酸 | |
| C. | 使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用 | |
| D. | 石油、煤、天然气、可燃冰、植物油都属于化石燃料 |
 ;
;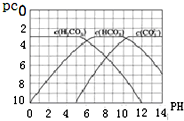 pC是指极稀溶液中溶质物质的量浓度的常用对数负值,类似pH.如某溶液溶质的浓度为1×10-3 mol•L-1,则该溶液中该溶质的pC=-lg10-3=3.已知H2CO3溶液中存在下列平衡:CO2+H2O?H2CO3 H2CO3?H++HCO3- HCO3-?H++CO32-.如图为H2CO3、HCO3-、CO32-在加入强酸或强碱溶液后,达到平衡时溶液中三种成分的pCpH图.
pC是指极稀溶液中溶质物质的量浓度的常用对数负值,类似pH.如某溶液溶质的浓度为1×10-3 mol•L-1,则该溶液中该溶质的pC=-lg10-3=3.已知H2CO3溶液中存在下列平衡:CO2+H2O?H2CO3 H2CO3?H++HCO3- HCO3-?H++CO32-.如图为H2CO3、HCO3-、CO32-在加入强酸或强碱溶液后,达到平衡时溶液中三种成分的pCpH图. H++HCO3-平衡向左移动放出CO2,碳酸浓度保持不变.
H++HCO3-平衡向左移动放出CO2,碳酸浓度保持不变.