题目内容
(8分)某化学小组设计实验验证温度对化学反应速率的影响。
【实验用品】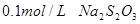 溶液、
溶液、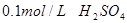 、烧杯、冷水、热水、秒表等
、烧杯、冷水、热水、秒表等
【实验步骤】
I.取两支试管各加入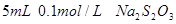 。
。
II. 另取两支试管各加入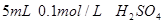 。
。
III. ……
IV. 一段时间后,分别混合并搅拌。
V. 记录实验现象及数据。
(1)步骤III的操作为 。
(2)该实验需要记录的实验数据是 。
(3)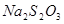 和
和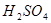 反应的化学方程式为 。
反应的化学方程式为 。
(4)能说明温度升高反应速率增大的现象是 。
【实验用品】
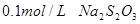 溶液、
溶液、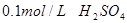 、烧杯、冷水、热水、秒表等
、烧杯、冷水、热水、秒表等【实验步骤】
I.取两支试管各加入
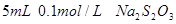 。
。II. 另取两支试管各加入
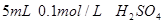 。
。III. ……
IV. 一段时间后,分别混合并搅拌。
V. 记录实验现象及数据。
(1)步骤III的操作为 。
(2)该实验需要记录的实验数据是 。
(3)
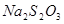 和
和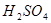 反应的化学方程式为 。
反应的化学方程式为 。(4)能说明温度升高反应速率增大的现象是 。
(8分)(每空2分)
(1)将四支试管分成两组(各有一支盛有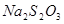 和
和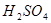 的试管),一组放入冷水中,另一组放入热水中。(一定要答出先分组浸泡,表述合理即可得分。若答为先混合,再分组浸泡不得分)
的试管),一组放入冷水中,另一组放入热水中。(一定要答出先分组浸泡,表述合理即可得分。若答为先混合,再分组浸泡不得分)
(2)出现浑浊的时间
(3)
(4)放入热水中的一组先出现浑浊
(1)将四支试管分成两组(各有一支盛有
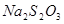 和
和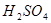 的试管),一组放入冷水中,另一组放入热水中。(一定要答出先分组浸泡,表述合理即可得分。若答为先混合,再分组浸泡不得分)
的试管),一组放入冷水中,另一组放入热水中。(一定要答出先分组浸泡,表述合理即可得分。若答为先混合,再分组浸泡不得分)(2)出现浑浊的时间
(3)

(4)放入热水中的一组先出现浑浊
(1)要验证温度对反应速率的影响,则需要进行对比实验,因此步骤Ⅲ是将四支试管分成两组(各有一支盛有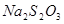 和
和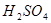 的试管),一组放入冷水中,另一组放入热水中。
的试管),一组放入冷水中,另一组放入热水中。
(2)由于反应中会产生单质硫沉淀,所以需要记录的实验数据是溶液出现混浊的时间。
(3)在酸性溶液中,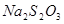 发生自身的氧化还原反应生成单质硫、SO2和水,方程式为
发生自身的氧化还原反应生成单质硫、SO2和水,方程式为 。
。
(4)温度高反应速率就快,所以出现混浊的时间就少。
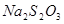 和
和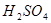 的试管),一组放入冷水中,另一组放入热水中。
的试管),一组放入冷水中,另一组放入热水中。(2)由于反应中会产生单质硫沉淀,所以需要记录的实验数据是溶液出现混浊的时间。
(3)在酸性溶液中,
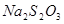 发生自身的氧化还原反应生成单质硫、SO2和水,方程式为
发生自身的氧化还原反应生成单质硫、SO2和水,方程式为 。
。(4)温度高反应速率就快,所以出现混浊的时间就少。

练习册系列答案
相关题目


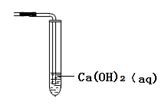



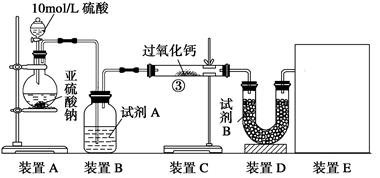
 油脂漂白及高温氧化剂,还可以作为鱼池增氧剂。将SO2通入过氧化钙固体粉末中有气体
油脂漂白及高温氧化剂,还可以作为鱼池增氧剂。将SO2通入过氧化钙固体粉末中有气体 钙的反应原理相同;但也有人提出:SO2具有较强的还原性,CO2无强还原性,反应原理不相同。据此设计如下实验操作进行判断
钙的反应原理相同;但也有人提出:SO2具有较强的还原性,CO2无强还原性,反应原理不相同。据此设计如下实验操作进行判断 。
。
 的体积
的体积