题目内容
关于化学反应中的能量变化,下列说法中不正确的是( )
| A.燃烧反应都是放热反应 |
B.对于可逆反应:aA(g)+bB(g) bC(g)+dD(g),如果正反应放热,逆反应一定吸热 bC(g)+dD(g),如果正反应放热,逆反应一定吸热 |
| C.氢气燃烧生成水是一个放热的化学反应,说明1 mol H2的能量高于1 mol H2O的能量 |
| D.只有放热的氧化还原反应才可以设计为原电池 |
C
解析试题分析:A、燃烧就是发光、放热的剧烈的氧化还原反应,正确;B、△H=生成物的能量和-反应物的能量和,所以其逆反应的反应热是其相反数,正确;C、氢气燃烧放热,说明氢气和氧气的能量和比水高,不能说明1 mol H2的能量高于1 mol H2O的能量,错误;D、反应物比生成物能量高时,才有能量转化为其他能量,正确。
考点:本题考查燃烧的概念、反应热及其求算。

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
关于晶体的叙述中,正确的是
| A.原子晶体中,共价键的键能越大,熔、沸点越高 |
| B.分子晶体中,分子间的作用力越大,该分子越稳定 |
| C.分子晶体中,共价键的键能越大,熔、沸点越高 |
| D.某晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体 |
已知反应A+B=C+D的能量变化如右图所示,下列说法正确的是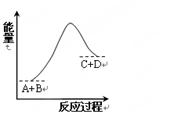
| A.该反应为放热反应 |
| B.该反应为吸热反应 |
| C.反应物的总能量高于生成物的总能量 |
| D.该反应只有在加热条件下才能进行 |
以下说法正确的是( )
| A.不能自发进行的反应属于吸热反应 |
| B.化学键断裂时吸收的能量大于化学键形成时放出的能量的反应属于放热反应 |
| C.升高反应的温度,活化分子百分数增加,分子间有效碰撞的几率提高,反应速率增大 |
| D.催化剂通过改变反应路径,使反应速率增大,但不改变反应所需的活化能 |
下列关于能源和作为能源的物质的叙述错误的是
| A.吸热反应的反应物总能量低于生成物总能量 |
| B.绿色植物进行光合作用时,将光能转化为化学能“贮存”起来 |
| C.物质的化学能可以在不同条件下转为热能、电能、光能等为人类所利用 |
| D.天然气属于二次能源 |
 C+D的能量变化如图所示,下列说法正确的是
C+D的能量变化如图所示,下列说法正确的是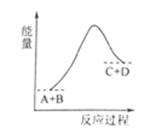
 kJ,破坏1mol氯气中的化学键消耗的能量为
kJ,破坏1mol氯气中的化学键消耗的能量为 kJ,形成1mol氯化氢中的化学键释放的能量为
kJ,形成1mol氯化氢中的化学键释放的能量为 kJ。下列关系式中正确的是( )
kJ。下列关系式中正确的是( )