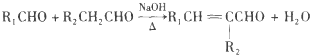��Ŀ����
 �Լ״�Ϊ���ȼ���ǽ���ҹ�ʯ����Դ��ȱ����Ҫ��ʩ��
�Լ״�Ϊ���ȼ���ǽ���ҹ�ʯ����Դ��ȱ����Ҫ��ʩ����1��CO��CO2�����ڼ״��ĺϳɣ�����ط�Ӧ���Ȼ�ѧ����ʽ���£�
CO��g��+2H2��g���TCH3OH��g����H=-102.5kJ?mol-1
CO��g��+H2O��g���TCO2��g��+H2��g����H=-42.9kJ?mol-1
��ӦCO2��g��+3H2��g���TCH3OH��g��+H2O��g����H=
��ӦCO��g��+H2O��g���TCO2��g��+H2��g����ƽ�ⳣ��K�ı���ʽΪ
��2����CO2�ϳɼ״�ʱ��ѡ���Ǹ���п��ZnCr2O4����CuClΪ������
�ٹ�ҵ�Ʊ��Ǹ���п����CO��ԭZnCrO4?H2O��ͬʱ����ZnO���÷�Ӧ�Ļ�ѧ����ʽ��
��CuCl�Dz�����ˮ�İ�ɫ���壬�Ʊ�ʱ��CuCl2��Һ�м������ͭ�ۣ�������ӦCuCl2+Cu�T2CuCl����ʵ�������Ӧ�ȼ���Ũ���ᣬ������ӦCuCl+HCl?H[CuCl2]����Ӧ��������Һ��������ˮ����CuCl���ɣ�ʵ������м���Ũ�����Ŀ����
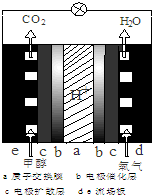
��3��ֱ�Ӽ״�ȼ�ϵ�ؽṹ��ͼ��ʾ������Ӧ��
���㣺�Ȼ�ѧ����ʽ,��ѧ��Դ���͵��,��ѧƽ�ⳣ���ĺ���,���ܵ���ʵ��ܽ�ƽ�⼰����ת���ı���
ר�⣺�����������������
��������1�����ݸ�˹���ɼ������Ȼ�ѧ����ʽ�������ӦCO2��g��+3H2��g���TCH3OH��g��+H2O��g���ġ�H�����ݻ�ѧƽ�ⳣ���ĸ������ʽд����ӦCO��g��+H2O��g���TCO2��g��+H2��g����ƽ�ⳣ��K�ı���ʽ��
��2���ٸ��������Ϣ���Ʊ��Ǹ���п����CO��ԭZnCrO4?H2O��ͬʱ����ZnO��ȷ����Ӧ������Ȼ��д����Ӧ�Ļ�ѧ����ʽ��������һ���¶��²��ܾ��н�ǿ�Ĵ����ԣ�
�ڸ���Ũ���ᷢ���ķ�Ӧ���ƽ���ƶ�ԭ�������ͣ�����CuCl��Ksp=c��Cu+��?c��Cl-�������c��Cu+����
��3��ȼ�ϵ���У�����ʧȥ���ӷ���������Ӧ���״��ڷ�Ӧ�б����������Ը�����ӦΪ�״�ʧȥ�������ɶ�����̼�ķ�Ӧ��
��2���ٸ��������Ϣ���Ʊ��Ǹ���п����CO��ԭZnCrO4?H2O��ͬʱ����ZnO��ȷ����Ӧ������Ȼ��д����Ӧ�Ļ�ѧ����ʽ��������һ���¶��²��ܾ��н�ǿ�Ĵ����ԣ�
�ڸ���Ũ���ᷢ���ķ�Ӧ���ƽ���ƶ�ԭ�������ͣ�����CuCl��Ksp=c��Cu+��?c��Cl-�������c��Cu+����
��3��ȼ�ϵ���У�����ʧȥ���ӷ���������Ӧ���״��ڷ�Ӧ�б����������Ը�����ӦΪ�״�ʧȥ�������ɶ�����̼�ķ�Ӧ��
���
�⣺��1����CO��g��+2H2��g���TCH3OH��g����H=-102.5kJ?mol-1
��CO��g��+H2O��g���TCO2��g��+H2��g����H=-42.9kJ?mol-1
���ݸ�˹���ɢ�-�ڿɵã�CO2��g��+3H2��g���TCH3OH��g��+H2O��g����H=-102.5kJ?mol-1-��-42.9kJ?mol-1��=-59.6kJ?mol-1��
��ӦCO��g��+H2O��g���TCO2��g��+H2��g����ƽ�ⳣ��K�ı���ʽΪ��K=
��
�ʴ�Ϊ��-59.6��K=
��
��2�����Ʊ��Ǹ���п��ZnCr2O4������CO��ԭZnCrO4?H2O��ͬʱ����ZnO����Ӧ�Ļ�ѧ����ʽΪ��2ZnCrO4?H2O+3CO=ZnO+ZnCr2O4+3CO2+2H2O��
������һ���¶��²��ܾ��н�ǿ�Ĵ����ԣ����Ǹ���пΪ����ʱ����ҵ�ϵ������¶��ǣ�350�桫420�棬˵����ʱ�����Ǹ���п�Ļ������
�ʴ�Ϊ��2ZnCrO4?H2O+3CO=ZnO+ZnCr2O4+3CO2+2H2O����ʱ�����Ǹ���п�Ļ�������¶����ߣ���Ӧ��������
���Ʊ�CuClʱ����CuCl2��Һ�м������ͭ�ۣ�������ӦCuCl2+Cu�T2CuCl����ʵ�������Ӧ�ȼ���Ũ���ᣬ������ӦCuCl+HCl?H[CuCl2]���ɴ˿ɼ�����Ũ������Դ�ʹƽ�������ƶ����������Է�ֹCuCl���帲����Cu���棬Ӱ�췴Ӧ�Ľ��У�
��c��Cl-��=2��10-3 mol?L-1ʱ��CuCl��Ksp=c��Cu+��?c��Cl-������c��Cu+��=
=
=8.5��10-5mol/L��
�ʴ�Ϊ����ʹƽ�������ƶ�����ֹCuCl���帲����Cu���棬Ӱ�췴Ӧ�Ľ��У�8.5��10-5��
��3��ȼ�ϵ���У���������������Ӧ���״��ڷ�Ӧ�б������ɶ�����̼�����Ը����缫��ӦΪ��CH3OH+H2O-6e-=CO2+6H+��
�ʴ�Ϊ��CH3OH+H2O-6e-=CO2+6H+��
��CO��g��+H2O��g���TCO2��g��+H2��g����H=-42.9kJ?mol-1
���ݸ�˹���ɢ�-�ڿɵã�CO2��g��+3H2��g���TCH3OH��g��+H2O��g����H=-102.5kJ?mol-1-��-42.9kJ?mol-1��=-59.6kJ?mol-1��
��ӦCO��g��+H2O��g���TCO2��g��+H2��g����ƽ�ⳣ��K�ı���ʽΪ��K=
| c(CO2)?c(H2) |
| c(CO)?c(H2O) |
�ʴ�Ϊ��-59.6��K=
| c(CO2)?c(H2) |
| c(CO)?c(H2O) |
��2�����Ʊ��Ǹ���п��ZnCr2O4������CO��ԭZnCrO4?H2O��ͬʱ����ZnO����Ӧ�Ļ�ѧ����ʽΪ��2ZnCrO4?H2O+3CO=ZnO+ZnCr2O4+3CO2+2H2O��
������һ���¶��²��ܾ��н�ǿ�Ĵ����ԣ����Ǹ���пΪ����ʱ����ҵ�ϵ������¶��ǣ�350�桫420�棬˵����ʱ�����Ǹ���п�Ļ������
�ʴ�Ϊ��2ZnCrO4?H2O+3CO=ZnO+ZnCr2O4+3CO2+2H2O����ʱ�����Ǹ���п�Ļ�������¶����ߣ���Ӧ��������
���Ʊ�CuClʱ����CuCl2��Һ�м������ͭ�ۣ�������ӦCuCl2+Cu�T2CuCl����ʵ�������Ӧ�ȼ���Ũ���ᣬ������ӦCuCl+HCl?H[CuCl2]���ɴ˿ɼ�����Ũ������Դ�ʹƽ�������ƶ����������Է�ֹCuCl���帲����Cu���棬Ӱ�췴Ӧ�Ľ��У�
��c��Cl-��=2��10-3 mol?L-1ʱ��CuCl��Ksp=c��Cu+��?c��Cl-������c��Cu+��=
| Ksp |
| c(Cl-) |
| 1.7��10-7 |
| 2��10-3 |
�ʴ�Ϊ����ʹƽ�������ƶ�����ֹCuCl���帲����Cu���棬Ӱ�췴Ӧ�Ľ��У�8.5��10-5��
��3��ȼ�ϵ���У���������������Ӧ���״��ڷ�Ӧ�б������ɶ�����̼�����Ը����缫��ӦΪ��CH3OH+H2O-6e-=CO2+6H+��
�ʴ�Ϊ��CH3OH+H2O-6e-=CO2+6H+��
���������⿼�����Ȼ�ѧ����ʽ����ѧ����ȼ�ϵ�ؼ�����ԭ������ѧƽ�ⳣ���ĸ������ʽ�����ܵ���ʵij����ܽ�ƽ�⣬��Ŀ�Ѷ��еȣ������漰��֪ʶ��϶࣬ע������ԭ��ع���ԭ������ѧƽ�ⳣ���ļ��㷽�����ܹ����ݸ�˹������дĿ���Ȼ�ѧ����ʽ��

��ϰ��ϵ�д�
�����Ŀ
 ��ѧ��������A��B��C��D��E��X��������ͼת����ϵ������������ͷ�Ӧ������ȥ���������ƶϲ���ȷ���ǣ�������
��ѧ��������A��B��C��D��E��X��������ͼת����ϵ������������ͷ�Ӧ������ȥ���������ƶϲ���ȷ���ǣ�������| A����DΪNaCl����A����C��Ӧ����B����E������CO2 |
| B����D��һ��ǿ���A��B��C������X��Ӧ����D |
| C����D��һ�ְ�ɫ�������ڿ��������ձ�ɺ��ɫ����A�������� |
| D����D��һ�����ᣬ��A�ȿ����ǵ��ʣ�Ҳ�����ǻ������D����ͭ��Ӧ����B��C |
��NAΪ�����ӵ�������ֵ������˵����ȷ���ǣ�������
| A��1L 0.1mol?L-1�İ�ˮ�к��е�NH3?H2O������Ϊ0.1NA |
| B����⾫��ͭʱ����������������6.4g�����·��ת�Ƶ�����Ϊ0.2NA |
| C����״���£�2.24L�Ķ��ȼ����к��е�̼�ȹ��ۼ�����ĿΪ0.2NA |
| D��һ�������£�4.6g NO2��N2O4��������к��е�Nԭ����ĿΪ0.1NA |
 ���������������ȵ������ҵ��µĴ�л�����ۺ�֢���Ը�Ѫ��Ϊ��Ҫ��־���������������ʳƷ��ȱ���˶�����������
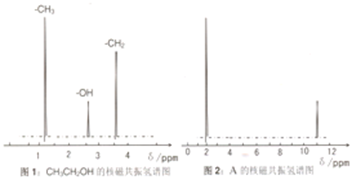
���������������ȵ������ҵ��µĴ�л�����ۺ�֢���Ը�Ѫ��Ϊ��Ҫ��־���������������ʳƷ��ȱ���˶�����������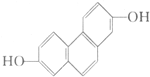 ���Ӻ˴Ź��������о��л�������ṹ�������ֶ�֮һ���ṹ�еĵ�Ч��ԭ�Ӻ˴Ź������ж���������Ӧ�ķ�ֵ ���źţ������з��ǿ����ṹ�е�Hԭ���������ȣ��Իش𣬽ṹ��ʽΪ��ͼ��ʾ���л������
���Ӻ˴Ź��������о��л�������ṹ�������ֶ�֮һ���ṹ�еĵ�Ч��ԭ�Ӻ˴Ź������ж���������Ӧ�ķ�ֵ ���źţ������з��ǿ����ṹ�е�Hԭ���������ȣ��Իش𣬽ṹ��ʽΪ��ͼ��ʾ���л������

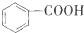 ��-R1��-R2��ʾ��ԭ�ӻ���������
��-R1��-R2��ʾ��ԭ�ӻ���������