��Ŀ����
��14�֣�������(��Ҫ�ɷ�ΪAl2O3��SiO2��Fe2O3)����ȡ��������ԭ�ϡ���ȡ�������Ĺ����������£�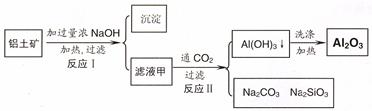
��1����Һ����Ҫ�ɷ��ǣ�д��ѧʽ�� ������������������������
��2��д����Ӧ II �����ӷ���ʽ��
��3����Ϸ�ӦII���ж�������������� ( H+) ����������ǿ������˳���� ������ĸ��ţ�
A��AlO2�D B��OH�D C��SiO32�D
��4��ȡ��Һ������������������ᣬ���ˣ����ö��Ե缫�������Һ���������������������ȫ���ݳ��������������г������ɣ���������ʧ��������ʧ��ԭ��������ӷ���ʽ��ʾΪ��
��5��ȡ ��4�� ����Ժ����Һ 10.0 mL��������������Һ��ֻ�������ֵ����ʵ���Ũ�ȵļ������ʣ���������μ���0.100 mol? L��1������Һ��������50.0mL ������Һʱ�����ɵij���ǡ���ܽ⡣
�ټ���50.0mL ������Һ���������ӷ�Ӧ���Ⱥ�˳������Ϊ��
���뻭�����ɳ��������ʵ����������������Ĺ�ϵͼ��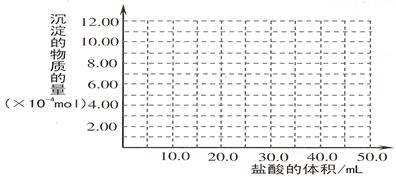
�š�NaOH��NaAlO2��Na2SiO3
�ơ�CO2+2OH��==CO32��+2H2O CO2��2H2O +2 AlO2��==2Al(OH)3��+HCO3��
�ǡ�b��a��c �ȡ�Al(OH)3 +OH����AlO2��+2H2O
�� �� H����OH��==H2O AlO2-��H��+H2O =Al(OH)3�� Al(OH)3��3H��=Al3����3H2O
��ͼ����������ʾ��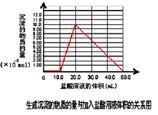
���������������1���������м��������NaOH��Һ�����е�Al2O3��SiO2������Ӧ�õ�NaAlO2��Na2SiO3������NaOH��Һ��������Һ����Ҫ�ɷ���NaAlO2��Na2SiO3��NaOH�������ԵĹ�����Fe2O3����2������NaAlO2��Na2SiO3��NaOH����Һ��ͨ�����CO2��������ӦCO2+2OH��=CO32��+2H2O ��CO2��2H2O +2AlO2��==2Al(OH)3��+HCO3�����õ�Al(OH)3��������3��H2O���������ʣ�Al(OH)3���������ʣ�H2SiO3�����ᡣ������������� ( H+) ����������ǿ������˳����b��a��c����4������NaAlO2��Na2SiO3��NaOH�ļ���������ᷢ����Ӧ�õ�AlCl3��NaCl��H2SiO3����ҺΪAlCl3��NaCl�Ļ����Һ���ö��Ե缫��⣬������������Ӧ��2H++2e-=H2��,�����ƻ��˸�����ˮ�ĵ���ƽ�⣬��Һ��OH-��Ũ������OH-����Һ�е�Al3+������Ӧ�γ�Al(OH)3������������������Ӧ��2Cl-��2e-=Cl2��������Һ�ʼ���ʱ���ַ�����Ӧ��Al(OH)3+ OH-= AlO2-+ 2H2O�����������ܽ����ʧ����5���ټ���50.0mL ������Һ���������ӷ�Ӧ���Ⱥ�˳����H����OH��=H2O ��AlO2-��H��+H2O =Al(OH)3�� Al(OH)3��3H��=Al3����3H2O �� ���ڶ��ߵ����ʵ�����ȣ��������Ƕ�����0.100 mol/L��0.01L=0.001mol��NaOH��HCl��Ӧ����10mlHCl; NaAlO2��HCl��Ӧ�γ�Al(OH)3��������10mlHCl;�ܽ�Al(OH)3��������30mlHCl.ͼ���ͼʾ:
���㣺����Ԫ���뻯��������ʡ������ķ��롢���ӷ���ʽ����д��n(HCl)������Ĺ�ϵͼ���֪ʶ��

 �����Ծ�ϵ�д�
�����Ծ�ϵ�д� �ο�����������100��ϵ�д�
�ο�����������100��ϵ�д�����Mg��Al��ɵ�һ�������Ļ����Ͷ��500 mL ϡ�����У�����ȫ���ܽⲢ�������塣����Ӧ��ȫ����������Һ�м���NaOH��Һ�����ɳ��������ʵ��������NaOH��Һ�������ϵ����ͼ��ʾ��������˵����ȷ����
| A��������Mg��Al��ɵĻ���������Ϊ8g |
| B����������ʵ���Ũ��Ϊ1 mol��L��1 |
| C�����ɵ�H2�ڱ�״���µ����Ϊ11.2L |
| D��NaOH��Һ�����ʵ���Ũ��Ϊ3.75 mol��L��1 |
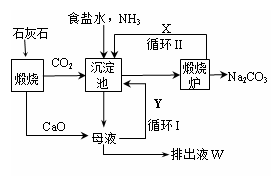
��12�֣�ij�о���ѧϰС���������Ѽ�����Ϣ���ء��ơ��ơ�þ�Ȼ��ý�������CO2������ȼ�ա����Ƕ�����CO2������ȼ�ս���������ʵ�飺
| �������� | ʵ������ |
| ������IJ���ȼ�ճ���ȼ�յ���Ѹ�� ���뵽ʢ��װ��CO2�ļ���ƿ�� | ����ʢ��CO2�ļ���ƿ�м���ȼ�� |
| ��Ӧ����ȴ | ����ƿ���ź�ɫ������ƿ���ϸ����а�ɫ ���� |
a��ˮ b����ĭ���� c����ɳ�� d��������̼
��2����С��ͬѧ��ƿ���ϵİ�ɫ���ʵijɷֽ������۲��������
I����ɫ������Na2O;
II����ɫ������Na2CO3;
III����ɫ���ʻ�������
��3��
| ʵ�鲽�� | ʵ������ |
| ��ȡ������ɫ�������Թ��У���������ˮ������Ʒȫ ������ˮ�������м��������CaCl2��Һ | ���ְ�ɫ���� |
| �ھ���Ƭ�̣�ȡ�ϲ���Һ���Թ��У��μ���ɫ��̪��Һ | ���������� |
��д���÷�Ӧ�ķ���ʽ ��
��15�֣�����ͭ�ڻ�����ũҵ�����кܹ㷺���ô���ij��ѧ��ȤС��������ϣ������ֲ�ͬ��ԭ����ȡ����ͭ��
��ʽһ��һ�ֺ�ͭ�Ŀ�ʯ�����ȸʯ��ۣ�����ͭ��̬ΪCuCO3��Cu(OH)2��CuSiO3��2H2O������SiO2��FeCO3��Fe2O3��Al2O3�����ʣ��������ֿ�ʯΪԭ����ȡ����ͭ�Ĺ�����������ͼ��
��ش��������⣺
����ɲ������ϡ������CuSiO3��2H2O������Ӧ�Ļ�ѧ����ʽ
CuSiO3��2H2O+H2SO4=CuSO4 +________+H2O��
�Ʋ���ڵ�����ҺpHѡ�õ�����Լ���__________________
A. CuO B. MgO C. FeCO3 D NH3��H2O
���й��������↑ʼ��������ȫ������pH���±���
| �������� | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| ��ʼ������pH | 3.3 | 1.5 | 6.5 | 4.2 |
| ������ȫ��pH | 5.2 | 3.7 | 9.7 | 6.7 |
����ҺBͨ������Ũ���������Ũ��Ϊԭ����һ�룩����ȴ�ᾧ���Եõ�CuSO4��5H2O���塣ijͬѧ��Ϊ������������������������������������������ݶԸ�ͬѧ�Ĺ۵��������ۣ���֪�����£�Al2(SO4)3 ������Һ��C(Al3+)=2.25mol��L-1��Ksp[Al(OH)3]=3.2��10-34) ________�����ȷ��������
��ʽ�����Ի�ͭ��Ϊԭ�ϣ���ȡ����ͭ������ͭ�Ĺ���������ʾ��
��.����ͭ����Ҫ�ɷ�ΪCuFeS2����������CaO��MgO��Al2O3������
��.��������װ�ý��е绯ѧ����ʵ�飬����ѡ��ͭ��ۼ�����������������ٽ��裬ʹ����ܽ⡣��������ͨ������������������������

��.һ��ʱ���ȡ��������Һ�������м����л���ȡ����RH��������Ӧ��
2RH���л��ࣩ+ Cu2+��ˮ�ࣩ
 R2Cu���л��ࣩ+ 2H����ˮ�ࣩ
R2Cu���л��ࣩ+ 2H����ˮ�ࣩ������л��࣬�����м���һ��Ũ�ȵ����ᣬʹCu2+����������
��.�������ͭ��Һ�Ƶý���ͭ��
��5����ͭ��ۼ��������������ἰ��������Ҫ�������·�Ӧ��
CuFeS2 + 4H�� = Cu2+ + Fe2+ + 2H2S 2Fe3+ + H2S = 2Fe2+ + S��+ 2H��
�������У�������Fe3+��Ũ�Ȼ������ֲ��䣬ԭ����____________________���õ缫��Ӧʽ��ʾ����
��6����������л����м���һ��Ũ�ȵ����ᣬCu2+����������ԭ����_____________ ��
��7��������������0.1mol CuSO4��Һ������ͭ3.2 g����ʱ��Һ������Ũ���ɴ�С��˳���� ____ ��
����������(��Ҫ��Fe2O3��SiO2��Al2O3��MgO������)�Ʊ��������Ĺ����������£�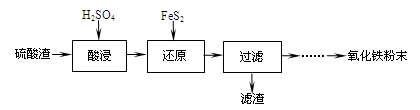
��1���������������Ҫ�ʵ�������Ŀ���ǣ���������Ľ����ʣ��� ��
��2������ԭ���ǽ�Fe3��ת��ΪFe2����ͬʱFeS2������ΪSO42�����÷�Ӧ�����ӷ���ʽΪ
��
��3��Ϊ�ⶨ��������������Һ��Fe3�������Կ��Ƽ���FeS2������ʵ�鲽��Ϊ��
ȷ��ȡһ���������������Һ����ƿ�У�����HCl���Թ���SnCl2���ټ�HgCl2��ȥ������SnCl2���Զ�����������Ϊָʾ������K2Cr2O7����Һ�ζ����йط�Ӧ����ʽ���£�
2Fe3����Sn2����6Cl����2Fe2����SnCl62����
Sn2����4Cl����2HgCl2��SnCl62����Hg2Cl2����
6Fe2����Cr2O72����14H����6Fe3����2Cr3����7H2O��
����SnCl2����������ⶨ��Fe3���� (�ƫ�ߡ�����ƫ�͡��������䡱����ͬ)��
��������HgCl2����ⶨ��Fe3���� ��
��4���ٿ�ѡ�� (���Լ�)������Һ�к���Fe3+������Fe3+��ԭ����
(�����ӷ�Ӧ����ʽ��ʾ)��
����֪����������������������ʽ����ʱ��Һ��pH���±���
| ������ | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | Mn(OH)2 |
| ��ʼ���� | 2.7 | 3.8 | 7.5 | 9.4 | 8.3 |
| ��ȫ���� | 3.2 | 5.2 | 9.7 | 12.4 | 9.8 |
a. ������ ��
b. ������ ��
c. ���룬ϴ�ӣ� d. ��ɣ���ĥ��


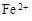 ��
��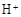 �⣬�����ܴ���������������������Ԫ�ط��ű�ʾ����
�⣬�����ܴ���������������������Ԫ�ط��ű�ʾ����