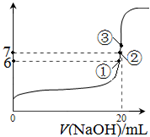
题目内容
已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1。回答有关中和反应的问题。
(1)用0.1 mol Ba(OH)2配成稀溶液与足量稀硝酸反应,能放出________kJ热量。
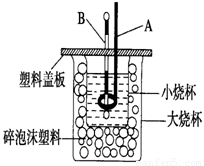
(2)如图装置中仪器A的名称是 ,碎泡沫塑料的作用是 。
(3)若通过实验测定中和热的ΔH,其结果常常大于-57.3 kJ·mol-1,其原因可能是
。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 (填“偏大”、“偏小”、“无影响”)。
(1)11.46
(2)环形玻璃搅拌棒;隔热,减少热量散失
(3)实验过程中难免有热量散失(合理答案均可)
(4)偏小
【解析】
试题分析:(1)由H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ·mol-1可知生成1molH2O放出热量为57.3kJ,而0.1mol Ba(OH)2 配成稀溶液与足量稀硝酸反应可得0.2molH2O,所以放出的热量为57.3kJ×0.2=11.46kJ,答案为:11.46;
(2)仪器A的名称是环形玻璃搅拌棒;中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎泡沫塑料的作用是:环形玻璃搅拌棒;隔热,减少热量散失,答案为:环形玻璃搅拌棒;隔热,减少热量散失;
(3)若保温效果不好,有热量散失,求得的中和热数值将会减小,△H大于-57.3kJ·mol-1,答案为:实验过程中难免有热量散失;(合理答案均可)
(4)醋酸为弱酸,电离过程为吸热过程,用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值偏小,故答案为:偏小;
考点:中和热的测定

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案 (2012?淄博一模)硫及其化合物在国民生产中占有重要的地位.
(2012?淄博一模)硫及其化合物在国民生产中占有重要的地位. ,下列说法正确的是
,下列说法正确的是 SO2Cl2(l)△H=-97.3kJ?mol-1
SO2Cl2(l)△H=-97.3kJ?mol-1