题目内容
16.下列各组物质中,含原子数最多的是( )| A. | 0.4 mol NH3 | B. | 4℃时5.4 mL水(水的密度为1g/cm3) | ||
| C. | 10 g氖气 | D. | 6.02×1023个硫酸分子 |
分析 A.1个氨气分子含有4个原子;
B.根据m=ρV计算水的质量,再根据n=$\frac{m}{M}$计算水的物质的量,1个水分子含有3个原子;
C.根据n=$\frac{m}{M}$计算氖的物质的量,氖为稀有气体,为单原子分子;
D.根据n=$\frac{N}{{N}_{A}}$计算硫酸的物质的量,1个硫酸分子含有7个原子.
解答 解:A.0.4molNH3含有0.4×4mol=1.6mol原子;
B.4℃时5.4mL水的质量为5.4mL×1g/mL=5.4g,物质的量为$\frac{5.4g}{18g/mol}$=0.3mol,水分子含有3个原子,故含有原子的物质的量为0.3mol×3=0.9mol;
C.10g氖的物质的量为$\frac{10g}{20g/mol}$=0.5mol,氖气是单原子分子,故氖原子物质的量为0.5mol;
D.6.02×1023个硫酸分子的物质的量为n=$\frac{N}{{N}_{A}}$=$\frac{6.02×1{0}^{23}}{6.02×1{0}^{23}}$=1mol,1个硫酸分子含有7个原子,故含原子数为7mol,
所以原子个数最多的是6.02×1023个硫酸分子,
故选D.
点评 本题考查物质的量的有关计算,比较基础,难度不大,注意对公式的理解,注意稀有气体是单原子分子.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
4.下列说法正确的是( )
| A. | 过氧化钠是既有氧化性又有还原性的淡黄色固体 | |
| B. | 铝箔在酒精灯上灼烧可观察到内部熔化但不滴落,说明铝的熔点高 | |
| C. | SiO2属于酸性氧化物,能和水化合生成硅酸 | |
| D. | 二氧化硅可以用来作太阳能电池的材料 |
11.下列化学反应符合“电解质(Ⅰ)+电解质(Ⅱ)═电解质(Ⅲ)+电解质(Ⅳ)”的是( )
| A. | Zn+H2SO4═ZnSO4+H2↑ | B. | CaCO3+2HNO3═Ca(NO3)2+CO2↑+H2O | ||
| C. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | D. | BaCl2+Na2SO4═2NaCl+BaSO4↓ |
8.设NA为阿伏加德罗常数的数值,则下列叙述不正确的是( )
| A. | 1 mol/L MgCl2溶液中含Cl-数为2NA | |
| B. | 标准状况下,2.24 L 18O2中所含中子的数目是2NA | |
| C. | 1 mol Al3+含有核外电子数为10NA | |
| D. | 常温常压下,16 g CH4中含有的原子总数为5NA |
5.有关钴和铁化合物的性质见下表
用含钴废料(含少量铁)可制备氯化钴:Co+2HCl═CoCl2+H2↑.工艺流程如下:
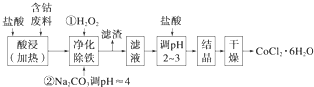
试回答:
(1)“净化除铁”中,写出加入H2O2时反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(2)②步中用Na2CO3调pH≈4的原因是碳酸钠可与盐酸反应,降低溶液的酸性,增大pH,使铁离子沉淀完全.
(3)“滤液”中所含主要溶质的化学式是CoCl2、NaCl、HCl.
(4)为防止CoCl2•6H2O脱水,“干燥”时可采用的方法或操作是减压烘干晶体表面的水分,或常温下晾干,或常温下鼓风吹干,或低于100度小心烘干等.
| 分子式 | 溶度积Ksp | 沉淀完全时的pH | 氯化钴晶体的性质 |
| Co(OH)2 | 5.9×10-15 | 9.4 | CoCl2•6H2O呈红色,常温下稳定.110~120℃时脱水变成蓝色无水氯化钴 |
| Fe(OH)2 | 1.6×10-14 | 9.6 | |
| Fe(OH)3 | 1.1×10-36 | 3.7 |

试回答:
(1)“净化除铁”中,写出加入H2O2时反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(2)②步中用Na2CO3调pH≈4的原因是碳酸钠可与盐酸反应,降低溶液的酸性,增大pH,使铁离子沉淀完全.
(3)“滤液”中所含主要溶质的化学式是CoCl2、NaCl、HCl.
(4)为防止CoCl2•6H2O脱水,“干燥”时可采用的方法或操作是减压烘干晶体表面的水分,或常温下晾干,或常温下鼓风吹干,或低于100度小心烘干等.

 氨在医药、化肥、国防、轻工业等方面均用途广泛.
氨在医药、化肥、国防、轻工业等方面均用途广泛.