题目内容
【题目】“绿水青山就是金山银山”,研究氮氧化物等大气污染物对建设美丽家乡,打造宜居环境具有重要意义。NO在空气中存在如下反应:2NO(g)+ O2(g)![]() 2NO2(g)△H上述反应分两步完成,如下左图所示。
2NO2(g)△H上述反应分两步完成,如下左图所示。
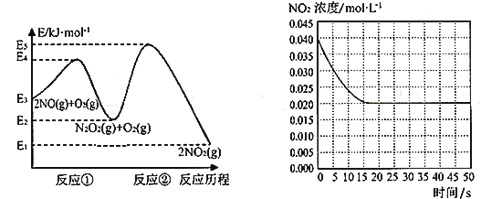
(1)写出反应①的热化学方程式(△H用含物理量E的等式表示):________。
(2)反应①和反应②中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。决定2NO(g)+O2(g)![]() 2NO2(g)反应速率的是____(填“反应①”或“反应②”);对该反应体系升高温度,发现总反应速率变慢,其原因可能是____(反应未使用催化剂)。
2NO2(g)反应速率的是____(填“反应①”或“反应②”);对该反应体系升高温度,发现总反应速率变慢,其原因可能是____(反应未使用催化剂)。
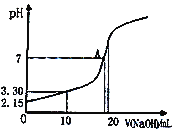
(3)某温度下一密闭容器中充入一定量的NO2,测得NO2浓度随时间变化的曲线如上图所示。前5秒内O2的平均生成速率为_______;该温度下反应2NO+O2![]() 2NO2的化学平衡常数K为_____。
2NO2的化学平衡常数K为_____。
(4)对于(3)中的反应体系达平衡后(压强为P1),若升高温度,再次达平衡后,混合气体的平均相对分子质量_____(填“增大”、“减小”或“不变”);若在恒温恒容条件下,向其中充入一定量O2,再次达平衡后,测得压强为P2,c(O2)=0.09mol·L-1,则P1︰P2=___________。
(5)水能部分吸收NO和NO2混合气体得到HNO2溶液。若向20.00mL0.10mol·L-1HNO2溶液中逐滴加入0.10mol·L-1NaOH溶液,所得pH曲线如图所示,则A点对应的溶液c(Na+)/c(HNO2)=____。
【答案】①2NO(g) ![]() N2O2(g) ΔH=(E2-E3)kJ·mol-1; 反应②; 决定总反应速率是反应②,温度升高后反应①平衡逆向移动,造成N2O2浓度减小,温度升高对于反应②的影响弱于N2O2浓度减小的影响,N2O2浓度减小导致反应②速率变慢; 0.001 mol·L-1·s-1; 100; 减少; 5:13; 103.70;
N2O2(g) ΔH=(E2-E3)kJ·mol-1; 反应②; 决定总反应速率是反应②,温度升高后反应①平衡逆向移动,造成N2O2浓度减小,温度升高对于反应②的影响弱于N2O2浓度减小的影响,N2O2浓度减小导致反应②速率变慢; 0.001 mol·L-1·s-1; 100; 减少; 5:13; 103.70;
【解析】
(1)根据图像反应①的热化学方程式为2NO(g) ![]() N2O2(g) ΔH=(E2-E3)kJ·mol-1。
N2O2(g) ΔH=(E2-E3)kJ·mol-1。
(2)根据图像反应①的活化能<反应②的活化能,反应①为快反应,反应②为慢反应,决定2NO(g)+O2(g)![]() 2NO2(g)反应速率的是慢反应②。对该反应体系升高温度,发现总反应速率变慢,其原因可能是:决定总反应速率是反应②,温度升高后反应①平衡逆向移动,造成N2O2浓度减小,温度升高对于反应②的影响弱于N2O2浓度减小的影响,N2O2浓度减小导致反应②速率变慢。
2NO2(g)反应速率的是慢反应②。对该反应体系升高温度,发现总反应速率变慢,其原因可能是:决定总反应速率是反应②,温度升高后反应①平衡逆向移动,造成N2O2浓度减小,温度升高对于反应②的影响弱于N2O2浓度减小的影响,N2O2浓度减小导致反应②速率变慢。
(3)前5s内υ(NO2)=(0.04mol/L-0.03mol/L)÷5s=0.002mol/(L·s),则υ(O2)=0.001mol/(L·s)。用三段式:
2NO2 ![]() 2NO+O2
2NO+O2
c(始)0.04 0 0
c(变)0.02 0.02 0.01
c(平)0.02 0.02 0.01
反应2NO2 ![]() 2NO+O2的平衡常数为(0.022×0.01)÷0.022=0.01,则反应2NO+O2
2NO+O2的平衡常数为(0.022×0.01)÷0.022=0.01,则反应2NO+O2 ![]() 2NO2的平衡常数K为1÷0.01=100。
2NO2的平衡常数K为1÷0.01=100。
(4)根据图像反应2NO2 ![]() 2NO+O2为吸热反应,对于(3)中的反应体系达平衡后(压强为P1),若升高温度,平衡正向移动,再次达平衡后,混合气体的质量不变,混合气体物质的量增大,混合气体的平均相对分子质量减小。再通入一定量O2,平衡逆向移动,设转化NO物质的量浓度为x,则平衡时NO2、NO、O2的浓度依次为(0.02+x)mol/L、(0.02-x)mol/L、0.09mol/L,温度不变平衡常数不变,则[(0.02-x)2×0.09]÷(0.02+x)2=0.01,解得x=0.01mol/L,即平衡时NO2、NO、O2的浓度依次为0.03mol/L、0.01mol/L、0.09mol/L,在恒温恒容时压强之比等于物质的量浓度之比,P1:P2=(0.02+0.02+0.01):(0.03+0.01+0.09)=5:13。
2NO+O2为吸热反应,对于(3)中的反应体系达平衡后(压强为P1),若升高温度,平衡正向移动,再次达平衡后,混合气体的质量不变,混合气体物质的量增大,混合气体的平均相对分子质量减小。再通入一定量O2,平衡逆向移动,设转化NO物质的量浓度为x,则平衡时NO2、NO、O2的浓度依次为(0.02+x)mol/L、(0.02-x)mol/L、0.09mol/L,温度不变平衡常数不变,则[(0.02-x)2×0.09]÷(0.02+x)2=0.01,解得x=0.01mol/L,即平衡时NO2、NO、O2的浓度依次为0.03mol/L、0.01mol/L、0.09mol/L,在恒温恒容时压强之比等于物质的量浓度之比,P1:P2=(0.02+0.02+0.01):(0.03+0.01+0.09)=5:13。
(5)根据图像0.1mol/LHNO2溶液的pH=2.15,则HNO2的电离平衡常数Ka=(1×10-2.15)2÷(0.1-1×10-2.15);A点溶液呈中性,c(H+)=c(OH-)=1×10-7mol/L,溶液中电荷守恒为c(H+)+c(Na+)=c(OH-)+c(NO2-),则A点溶液中c(Na+)=c(NO2-),A点对应的溶液中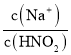 =
= =Ka÷c(H+)=[(1×10-2.15)2÷(0.1-1×10-2.15)]÷(1×10-7)=103.70。
=Ka÷c(H+)=[(1×10-2.15)2÷(0.1-1×10-2.15)]÷(1×10-7)=103.70。

 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案【题目】实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
Ⅰ 制备K2FeO4(夹持装置略)
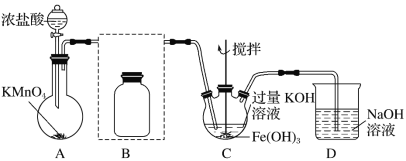
(1)A的作用_____________
(2)在答题纸上将除杂装置B补充完整并标明所用试剂:________
(3)在C中得到紫色固体的化学方程式为:______________
Ⅱ探究K2FeO4的性质:取C中紫色溶液,加入稀硫酸,产生气体和溶液a。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色 |
方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶解,得到紫色溶液b,取少量b,滴加盐酸,有Cl2产生 |
(4)由方案Ⅰ中溶液变红可知a中含有_____离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由_______产生(用离子方程式表示)。
(5)根据方案Ⅱ得出:氧化性Cl2________FeO42- (填“>”或“<”),而K2FeO4的制备实验实验表明,Cl2和FeO42-的氧化性强弱关系相反,原因是______。


