题目内容
10.下列实验或反应中,最后固体质量增加的是( )| A. | 铜丝在空气中灼烧后迅速伸入乙醇蒸气中 | |
| B. | 铁粉与硫粉物质的量之比为1:1时混合加热 | |
| C. | 锌粉加入到氯化铜溶液中 | |
| D. | 去除氧化膜的铝条插入到浓硝酸中 |
分析 A、铜灼烧生成了氧化铜,氧化铜和乙醇反应生成了乙醛和铜;
B、铁粉与硫粉反应生成硫化亚铁;
C、锌和硫酸铜发生置换反应生成铜和硫酸锌,固体质量减小;
D、铝在浓硝酸中常温下发生钝化,氧化铝是两性氧化物溶于浓硝酸.
解答 解:A、由于氧化铜能够和乙醇反应生成乙醛和铜,铜变成氧化铜,氧化铜又被还原成铜,最终铜质量没有变化,故A错误;
B、铁粉与硫粉反应生成硫化亚铁,铁粉与硫粉物质的量之比为1:1时恰好反应生成硫化亚铁,反应物质量不变,故B错误;
C、锌和硫酸铜发生置换反应生成铜和硫酸锌,Zn+Cu2+=Cu+Zn2+,固体质量减小,故C错误;
D、铝在浓硝酸中常温下发生钝化,氧化铝是两性氧化物溶于浓硝酸,去除氧化膜的铝条可以插入到浓硝酸中,故D正确;
故选D.
点评 本题考查了物质性质的分析判断,注意反应前后固体质量的变化分析,掌握常温下铝在浓硝酸中钝化和化学基础是关键,题目较简单.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
18.下列说法正确的是( )
| A. | 原子及其离子的核外电子层数等于该元素所在的周期数 | |
| B. | 元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素 | |
| C. | 所含质子数和电子数都相同的粒子一定是分子 | |
| D. | 同一元素的各种同位素的物理性质、化学性质均相同 |
15.铁铜单质及其化合物的应用范围很广.现有含氯化亚铁杂质的氯化铜晶体,为制取纯净的CuCl2•2H2O,首先将其制成水溶液,然后按照如图步骤进行提纯:

已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
请回答下列问题:
(1)化学上通常认为残留在溶液中的离子浓度小于1×10-5mol/L时,沉淀就达到完全.已知Fe(OH)2的Ksp约为1.0×10-15,则a=9.
(2)加入氧化剂的目的是将Fe2+氧化成Fe3+,X应选择C.
A.K2Cr2O7 B.浓HNO3 C.H2O2 D.KMnO4
(3)加入的物质Y是CuO[Cu(OH)2、CuCO3、Cu2(OH)2CO3也可以].
(4)设计实验从溶液Ⅲ中获得纯净的CuCl2•2H2O.简要描述实验步骤应在HCl气流中加热蒸发结晶,过滤、冰水洗涤、低温烘干.

已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| Fe3+ | Fe2+ | Cu2+ | |
| 开始沉淀的pH | 1.9 | 7.0 | 4.7 |
| 完全沉淀的pH | 3.2 | a | 6.7 |
(1)化学上通常认为残留在溶液中的离子浓度小于1×10-5mol/L时,沉淀就达到完全.已知Fe(OH)2的Ksp约为1.0×10-15,则a=9.
(2)加入氧化剂的目的是将Fe2+氧化成Fe3+,X应选择C.
A.K2Cr2O7 B.浓HNO3 C.H2O2 D.KMnO4
(3)加入的物质Y是CuO[Cu(OH)2、CuCO3、Cu2(OH)2CO3也可以].
(4)设计实验从溶液Ⅲ中获得纯净的CuCl2•2H2O.简要描述实验步骤应在HCl气流中加热蒸发结晶,过滤、冰水洗涤、低温烘干.
2.工业精炼铜的如图所示(如图),下列有关说法正确的是( )


| A. | 右边电极材料为精铜 | |
| B. | 电解质溶液可选择CuSO4溶液 | |
| C. | 随着电解的进行,溶液中Cu2+浓度逐渐增加 | |
| D. | 阳极质量的减小量等于阴极质量的增加量 |
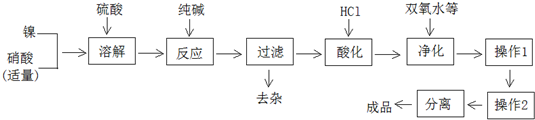
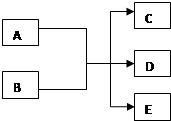 在一定条件下,某些化学反应可以如图框架表示(未注明反应条件),根据要求回答下列问题:
在一定条件下,某些化学反应可以如图框架表示(未注明反应条件),根据要求回答下列问题: