题目内容
【题目】为研究1.0mol/LFe(NO3)3溶液与Cu的反应,甲与乙做了如下实验:将Cu片放入1.0mol/L的Fe(NO3)3溶液中,观察到Cu片逐渐溶解,溶液变为蓝绿色,由此甲得出结论:Fe(NO3)3溶液中的Fe3+氧化了Cu。而乙认为,Fe(NO3)3溶液显酸性,此酸性条件下,NO3-也能氧化Cu。
(1)甲为证明自己的观点,设计如下实验:
步骤 | 操作 | 现象 |
Ⅰ | 取蓝绿色溶液,向其中加入K3[Fe(CN)6]溶液 | …… |
①请用离子方程式解释,Fe(NO3)3溶液显酸性的原因__________。
②证明甲观点正确的现象是__________,Fe3+与Cu反应的离子方程式为__________。
(2)乙证明自己的观点,设计如下实验:
步骤 | 操作 | 现象 |
Ⅱ | 用pH试纸测定1.0mol/L的Fe(NO3)3溶液的pH值 | 1.0mol/L的Fe(NO3)3溶液的pH=1 |
Ⅲ | 将1.0mol/L的Fe(NO3)3溶液替换为某种溶液(或混合溶液),加入Cu | …… |
①下列溶液中,可以用于替换上述Fe(NO3)3溶液的是__________(填序号)
a.0.1mol/LHNO3溶液
b.0.1mol/LFeCl3溶液
c.6.0mol/LNaNO3和0.2mol/L盐酸等体积混合后的溶液
②测定溶液pH值的操作是__________。
③乙查阅资料:NO3-在不同条件下的还原产物较复杂,有时难以观察到气体产生。证明乙观点正确的现象是__________。
(3)研究发现,甲和乙的观点都正确。丙得出结论:将Cu片放入1.0mol/L的Fe(NO3)3溶液中,Fe3+和NO3-均氧化的Cu。你是否同意丙的结论,理由是__________。
(4)为进一步研究1.0mol/LFe(NO3)3溶液与Cu的反应,甲与乙查阅资料:
水解反应 | 平衡常数(K) |
Fe3++3H2O | 7.9×10-4 |
Fe2++2H2O | 3.2×10-10 |
Cu2++2H2O | 3.2×10-7 |
甲与乙再次将Cu片放入1.0mol/L的Fe(NO3)3溶液中,并监测实验过程中溶液pH值的变化。他们发现Cu片逐渐溶解,溶液变为蓝绿色,且pH值略有上升。由此可以得出结论:__________。
【答案】 Fe3++3H2O![]() Fe(OH)3+3H+; 产生特征蓝色沉淀 2Fe3++Cu=Cu2++2Fe2+ c 用洁净的玻璃棒蘸取1.0mol/L的Fe(NO3)3溶液,点在pH试纸上,并与标准比色卡比对 (Cu溶解)溶液变为蓝色 不同意;甲同学检验出了Fe2+,可确定Fe3+一定氧化了Cu;乙同学虽然验证了此条件下NO3-能氧化Cu,但在硝酸铁溶液氧化Cu时,由于没有检验NO3-的还原产物,因此不能确定NO3-是否氧化了Cu Fe(NO3)3溶液中的Fe3+氧化了Cu
Fe(OH)3+3H+; 产生特征蓝色沉淀 2Fe3++Cu=Cu2++2Fe2+ c 用洁净的玻璃棒蘸取1.0mol/L的Fe(NO3)3溶液,点在pH试纸上,并与标准比色卡比对 (Cu溶解)溶液变为蓝色 不同意;甲同学检验出了Fe2+,可确定Fe3+一定氧化了Cu;乙同学虽然验证了此条件下NO3-能氧化Cu,但在硝酸铁溶液氧化Cu时,由于没有检验NO3-的还原产物,因此不能确定NO3-是否氧化了Cu Fe(NO3)3溶液中的Fe3+氧化了Cu
【解析】(1)①Fe3+的水解,使Fe(NO3)3溶液显酸性,发生水解反应的离子方程式为Fe3++3H2O![]() Fe(OH)3+3H+;
Fe(OH)3+3H+;
②取蓝绿色溶液,向其中加入K3[Fe(CN)6]溶液,产生特征蓝色沉淀,说明溶液里有Fe2+,即Cu还原Fe3+生成Fe2+,发生反应的离子方程式为2Fe3++Cu=Cu2++2Fe2+;
(2)①乙同学观点是在酸性条件下Cu与NO3-反应,实验中c(NO3-)=3mol/L,则可用6.0molL-1NaNO3和0.2molL-1盐酸等体积混合的溶液代替,而0.1mol/LHNO3溶液中NO3-浓度不够,0.1mol/LFeCl3溶液中无NO3-,故答案为c;
②用pH试纸测定溶液pH值的操作是用洁净的玻璃棒蘸取1.0mol/L的Fe(NO3)3溶液,点在pH试纸上,并与标准比色卡比对;
③依据乙的观念应该会观察到Cu溶解,溶液变为蓝色;
(3)甲同学检验出了Fe2+,可确定Fe3+一定氧化了Cu;乙同学虽然验证了此条件下NO3-能氧化Cu,但在硝酸铁溶液氧化Cu时,由于没有检验NO3-的还原产物,不能确定NO3-是否氧化了Cu,故不同意丙的结论;
(4)由图表可知Fe3+的水解能力明显强于Fe2+和Cu2+,Cu片放入1.0mol/L的Fe(NO3)3溶液中,Cu片逐渐溶解,溶液变为蓝绿色,且pH值略有上升,说明Fe3+氧化Cu,变为Cu2+和Fe2+,水解能力下降,导致实验过程中溶液pH略有上升,即 Fe(NO3)3溶液中的Fe3+氧化了Cu,而不是NO3-在酸性条件下氧化了Cu。

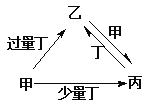
【题目】甲、乙、丙、丁均为中学化学中常见的单质或化合物,它们之间的转化关系如下图所示(部分产物已略去),下列各组物质中不能按图示关系转化的是
选项 | 物质转化关系 | 甲 | 乙 | 丙 | 丁 |
A |
| NaOH | NaHCO3 | Na2CO3 | CO2 |
B | AlCl3 | NaAlO2 | Al(OH)3 | NaOH | |
C | Fe | Fe(NO3)3 | Fe(NO3)2 | HNO3 | |
D | C | CO | CO2 | O2 |