题目内容
10.早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成.回答下列问题:(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过X-射线衍射方法区分晶体、准晶体和非晶体.
(2)基态Fe原子核外处在能量最高的能级上的电子共有6种不同的运动状态;Fe2+的价电子排布式为3d6,可用K3[Fe(CN)6]来检验Fe2+,形成的配合物的颜色为特征蓝色,其中[Fe(CN)6]3-配离子中的配原子是C.
(3)新制备的Cu(OH)2可将乙醛(CH3CHO)氧化成乙酸,而自身还原成Cu2O.乙醛中碳原子的杂化轨道类型为sp3、sp2,1mol乙醛分子中含有的σ键的数目为6NA.乙酸的沸点明显高于乙醛,其主要原因是CH3COOH存在分子间氢键.Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有16个铜原子.
(4)Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为12.列式表示Al单质的密度$\frac{4×27}{6.022×1023×(0.405×10-7)3}$g•cm-3(不必计算出结果).
分析 (1)晶体对X射线发生衍射,非晶体不发生衍射,准晶体介于二者之间;
(2)根据Fe原子的核外电子排布式确定未成对电子数,失去电子变为亚铁离子时,失去4s上的电子后形成,亚铁离子遇到K3[Fe(CN)6]变化为特征蓝色,其中[Fe(CN)6]3-配离子中的配原子为碳原子;
(3)乙醛中甲基上的C采取sp3杂化类型,醛基中的C采取sp2杂化类型;1个乙醛分子含有6个σ键和一个π键;乙酸分子间可形成氢键导致沸点较高;根据O数目和Cu2O中Cu和O的比例计算晶胞中Cu原子的数目;
(4)在Al晶体的一个晶胞中与它距离相等且最近的Al原子在通过这个顶点的三个面心上,面心占$\frac{1}{2}$,通过一个顶点可形成8个晶胞.
解答 解:(1)从外观无法区分三者,但用X光照射挥发现:晶体对X射线发生衍射,非晶体不发生衍射,准晶体介于二者之间,因此通过有无衍射现象即可确定,
故答案为:X射线衍射;
(2)26号元素Fe基态原子核外电子排布式为1s22s22p63s23p63d64s2,基态Fe原子核外处在能量最高的能级为3d,排布了6个电子,有6种不同的运动状态,可知在3d上存在4个未成对电子,失去电子变为亚铁离子时,失去4s上的2个电子后形成,因此Fe2+的价电子排布式为3d6,可用K3[Fe(CN)6]来检验Fe2+,形成的配合物的颜色为特征蓝色,其中[Fe(CN)6]3-配离子中的配原子为碳原子,
故答案为:6;3d6;特征蓝色;C;
(3)乙醛中甲基上的C形成4条σ键,无孤电子对,因此采取sp3杂化类型,醛基中的C形成3条σ键和1条π键,无孤电子对,采取sp2杂化类型;1个乙醛分子含有6个σ键和一个π键,则1mol乙醛含有6molσ键,即6NA个σ键;乙酸分子间可形成氢键,乙醛不能形成氢键,所以乙酸的沸点高于乙醛;该晶胞中O原子数为4×1+6×$\frac{1}{2}$+8×$\frac{1}{8}$=8,由Cu2O中Cu和O的比例可知该晶胞中铜原子数为O原子数的2倍,即为16个;
故答案为:sp3、sp2;6NA;乙酸存在分子间氢键;16;
(4)在Al晶体的一个晶胞中与它距离相等且最近的Al原子在通过这个顶点的三个面心上,面心占$\frac{1}{2}$,通过一个顶点可形成8个晶胞,因此该晶胞中铝原子的配位数为8×3×$\frac{1}{2}$=12;一个晶胞中Al原子数为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,因此Al的密度ρ=$\frac{m}{V}$=$\frac{4×27}{{N}_{A}×(0.405×1{0}^{-7})^{3}}$=$\frac{4×27}{6.02×1{0}^{23}×(0.405×1{0}^{-7})^{3}}$g•cm-3,
故答案为:12,$\frac{4×27}{6.02×1{0}^{23}×(0.405×1{0}^{-7})^{3}}$;
点评 本题考查了晶体的性质、原子核外电子排布规律、共价键类型、氢键、杂化类型、晶胞配位数及密度的计算,综合性非常强,为历年高考选作常考题型,难度中等,其中晶胞配位数以及密度的计算是本题的难点.

| 事实 | 解释或结论 | |
| A | 常温下铁、铝均不溶于浓硫酸 | 常温下铁、铝与浓硫酸均不反应 |
| B | 测定同浓度的Na2CO3溶液的pH小于Na2SiO3溶液的pH | 非金属性:C<Si |
| C | 向某溶液中加入2滴KSCN浓液、溶液不显红色;再向溶液中加入几滴新制氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
| D | 用浓、稀硝酸分别完全溶解等质量的铜粉,参加反应的硝酸的物质的量比较:稀硝酸中的<浓硝酸中的 | 稀硝酸氧化性比浓硝酸强 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 产物H20所具有的总能量高于反应物H2和O2所具有的总能量 | |
| B. | 反应物H2所具有的能量高于产物H2O所具有的总能量 | |
| C. | 反应物H2和O2所具有的总能量高于产物H2O所具有的总能量 | |
| D. | 反应物H2和02具有的能量相等 |
| A. | Cu和Al | B. | Mg和Al | C. | Al和 Zn | D. | Mg 和 Zn |
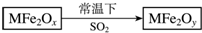 新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中化合价不发生变化.常温下,MFe2Ox能使工业废气中的SO2转化为S,流程如图,则下列判断正确的是( )
新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中化合价不发生变化.常温下,MFe2Ox能使工业废气中的SO2转化为S,流程如图,则下列判断正确的是( )| A. | MFe2Ox是氧化剂 | B. | SO2是该反应的催化剂 | ||
| C. | x<y | D. | MFe2Oy是还原产物 |
| A. | 大量使用煤发电是形成雾霾的主要原因之一 | |
| B. | 对“地沟油”蒸馏可以获得汽油 | |
| C. | 对废旧电池进行回收处理主要为了防止重金属污染水源 | |
| D. | 半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是硅 |
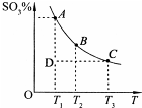 硫酸的年产量可以用来衡量一个国家的化工生产能力.工业生产硫酸的流程中存在反应:2SO2(g)+O2(g)?2SO3(g).反应体系中SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题:
硫酸的年产量可以用来衡量一个国家的化工生产能力.工业生产硫酸的流程中存在反应:2SO2(g)+O2(g)?2SO3(g).反应体系中SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题:
 ;
;