题目内容
11.NA为阿伏伽德罗常数的值.下列说法正确的是( )| A. | 18g D2O和18g H2O中含有的质子数均为10NA | |
| B. | PH=1的亚硫酸溶液中含有的H+数目为0.1NA | |
| C. | 2.3 g金属钠与过量的氧气反应,无论加热与否转移电子数均为0.1Na | |
| D. | 0.1 mol的Na2O2中含阴离子数是0.2 NA |
分析 A、重水的摩尔质量为20g/mol;
B、溶液体积不明确;
C、求出钠的物质的量,然后根据反应后钠变为+1价来分析;
D、过氧化钠由2个钠离子和1个过氧根构成.
解答 解:A、重水的摩尔质量为20g/mol,故18g重水的物质的量n=$\frac{18g}{20g/mol}$=0.9mol,而1mol重水中含10mol质子,故0.9mol水中含9mol质子即9NA个,故A错误;
B、溶液体积不明确,故溶液中氢离子的个数不能计算,故B错误;
C、2.3g钠的物质的量为0.1mol,而反应后钠变为+1价,故0.1mol钠转移0.1mol电子即0.1NA个,与生成的产物无关,故C正确;
D、过氧化钠由2个钠离子和1个过氧根构成,故0.1mol过氧化钠中含0.1mol阴离子即0.1NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
1.下列说法中正确的是( )
| A. | 胶体区别于其它分散系的本质特性是丁达尔现象 | |
| B. | 利用半透膜可除去淀粉溶液中的少量NaCl | |
| C. | Fe(OH)3胶体带正电荷 | |
| D. | 加入电解质,胶体一定能发生凝聚 |
2.化学是你,化学是我,化学深入我们生活.下列说法正确的是( )
| A. | 木材纤维和土豆淀粉遇碘水均显蓝色 | |
| B. | 包装用材料聚乙烯和聚氯乙烯都属于烃 | |
| C. | 食用花生油和鸡蛋清都能发生水解反应 | |
| D. | PX项目的主要产品对二甲苯属于饱和烃 |
6.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 60g丙醇中存在的共价键总数为10NA | |
| B. | 50mL 18.4 mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA | |
| C. | 钠在空气中燃烧可生成多种氧化物.23 g钠充分燃烧时转移电子数为1 NA | |
| D. | 235 g核素${\;}_{92}^{239}$U发生裂变反应:${\;}_{92}^{239}$U+${\;}_{0}^{1}$n$\stackrel{裂变}{→}$${\;}_{38}^{90}$Sr+${\;}_{54}^{136}$U+10${\;}_{0}^{1}$n净产生的中子(${\;}_{0}^{1}$n)数为10NA |
16.当把晶体N2O4放入恒容的密闭容器内,待全部气化并建立N2O4?2NO2平衡后,保持温度不变,再加入N2O4晶体并全部气化,待反应达到新的平衡,新平衡与旧平衡比较,其值减小的是( )
| A. | c(NO2) | B. | c(N2O4) | C. | $\frac{c(N{O}_{2})}{c({N}_{2}{O}_{4})}$ | D. | $\frac{c({N}_{2}{O}_{4})}{{c}^{2}(N{O}_{2})}$ |
7.有下列两种转化途径,某些反应条件和产物已省略,下列有关说法不正确的是( )
途径①S$\stackrel{农硝酸}{→}$H2SO4
途径②S$\stackrel{O_{2}}{→}$SO2$\stackrel{O_{2}}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4.
途径①S$\stackrel{农硝酸}{→}$H2SO4
途径②S$\stackrel{O_{2}}{→}$SO2$\stackrel{O_{2}}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4.
| A. | 途径①反应中体现了浓HNO3的强氧化性和酸性 | |
| B. | 途径②的第二步反应在实际生产中可以通过增大O2浓度来降低成本 | |
| C. | 由途径①和②分别制取1 mol H2SO4,理论上各消耗1 mol S,各转移6 mol e- | |
| D. | 途径②与途径①相比更能体现“绿色化学”的理念是因为途径②比途径①污染相对小且原子利用率高 |
4.将2molX 和2molY充入2L密闭容器中发生反应:X(g)+3Y(g)?2Z(g)+aQ(g).2min后达到平衡时生成0.8molZ,测得Q的浓度为0.6mol/L,下列叙述错误的是( )
| A. | a的值为3 | B. | 平衡时X的浓度为0.8mol/L | ||
| C. | Y的转化率为60% | D. | 反应速率v(Y)=0.2mol/(L•min) |
5.下列有关物质的分类合理的是( )
| A. | C60、HD均属于单质 | B. | 漂白粉、明矾均属于混合物 | ||
| C. | 氯化铵、硫酸均属于离子化合物 | D. | SO2、NxOy均属于酸性氧化物 |
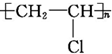 单体为CH2═CH-Cl.
单体为CH2═CH-Cl.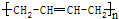 单体为CH2═CH-CH═CH2,
单体为CH2═CH-CH═CH2,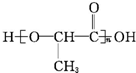 单体为
单体为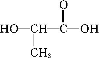 ,
,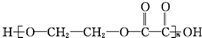 单体为HO-CH2CH2-OH和HOOC-COOH.
单体为HO-CH2CH2-OH和HOOC-COOH.