题目内容
C、Si、S都是自然界中含量丰富的非金属元素,下列关于其单质及化合物的说法中正确的是
A.三种元素在自然界中既有游离态又有化合态
B.二氧化物都属于酸性氧化物,能与碱反应而不能与任何酸反应
C.最低价的气态氢化物都具有还原性,易与O2发生反应
D.其最高价氧化物对应水化物的酸性强弱:H2SO4>H2SiO3>H2CO3
A.三种元素在自然界中既有游离态又有化合态
B.二氧化物都属于酸性氧化物,能与碱反应而不能与任何酸反应
C.最低价的气态氢化物都具有还原性,易与O2发生反应
D.其最高价氧化物对应水化物的酸性强弱:H2SO4>H2SiO3>H2CO3
C
试题分析:A、Si元素在自然界中无游离态,错误;B、SiO2能与HF反应,错误;C、C、Si、S低价态气态氢化物为CH4、SiH4、H2S,都具有还原性,易与O2发生反应,正确;D、根据元素性质的递变性,最高价氧化物对应水化物的酸性强弱:H2SO4>H2CO3>H2SiO3,错误。

练习册系列答案
相关题目
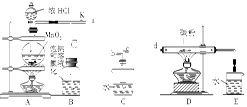
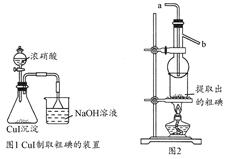
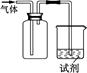
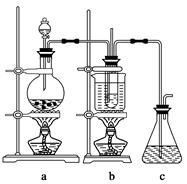
 5NaCl+NaClO3+3H2O,请推测在加热NaClO溶液时发生反应的化学方程式:______________________________。
5NaCl+NaClO3+3H2O,请推测在加热NaClO溶液时发生反应的化学方程式:______________________________。