题目内容
17.下列各组中两种物质在水溶液中的反应,可用同一离子方程式表示的是( )| A. | NaHCO3+HNO3;Na2CO3+HCl | B. | Cu(OH)2+HCl;Cu(OH)2+CH3COOH | ||
| C. | NaOH+H2SO4;KOH+NaHSO4 | D. | Na2CO3+HCl(少量);Na2CO3(少量)+HCl |
分析 A.NaHCO3电离出HCO3-,Na2CO3电离出CO32-;
B.CH3COOH为弱酸,应写成化学式,HCl为强电解质,写成离子;
C.反应的实质为OH-和H+的反应;
D.HCl少量生成碳酸氢钠,碳酸钠少量生成水、二氧化碳.
解答 解:A.NaHCO3电离出HCO3-,Na2CO3电离出CO32-,反应物不同,离子方程式不同,故A错误;
B.反应的离子方程式分别为:Cu(OH)2+2H+=Cu2++2H2O、Cu(OH)2+2CH3COOH=Cu2++2H2O+2CH3COO-,二者不同,故B错误;
C.反应的实质为OH-和H+的反应,离子反应均为OH-+H+=H2O,故C正确;
D.离子反应分别为CO32-+H+=HCO3-、CO32-+2H+=H2O+CO2↑,故D错误;
故选C.
点评 本题考查离子方程式的书写,为高频考点,注意判断反应物和生成物、强弱电解质等,把握发生的反应及离子反应的书写方法为解答的关键,题目难度不大.

练习册系列答案
相关题目
7.下列物质久置空气中会发生相应的变化,其中发生了氧化还原反应的是( )
| A. | 澄清的石灰水变浑浊 | B. | 浓硫酸的质量增重 | ||
| C. | 氢氧化钠的表面发生潮解 | D. | 铝的表面生成致密的薄膜 |
5.下列四个原电池的有关说法正确的是( )


| A. | 装置①中SO42-的向Al片移动 | |
| B. | 装置②中的Mg片上发生的反应为:2H++2e-═H2↑ | |
| C. | 装置③中铁片被氧化,铜片上产生气体 | |
| D. | 装置④中若有1摩尔铁锈(氧化铁)生成,理论上有4摩尔电子通过导线 |
9.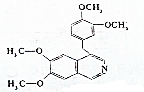 鸦片最早用于药物(有止痛、止泻、止渴作用),长期服用会成瘾,使人体质衰弱、精神颓废、寿命缩短.鸦片具有复杂的组成,其中的罂粟碱的分子结构如图所示:已知该物质的燃烧产物为CO2、H2O和N2,1mol该化和物完全燃烧的耗氧量及在一定条件下与H2发生加成反应的耗氢量分别为( )
鸦片最早用于药物(有止痛、止泻、止渴作用),长期服用会成瘾,使人体质衰弱、精神颓废、寿命缩短.鸦片具有复杂的组成,其中的罂粟碱的分子结构如图所示:已知该物质的燃烧产物为CO2、H2O和N2,1mol该化和物完全燃烧的耗氧量及在一定条件下与H2发生加成反应的耗氢量分别为( )
 鸦片最早用于药物(有止痛、止泻、止渴作用),长期服用会成瘾,使人体质衰弱、精神颓废、寿命缩短.鸦片具有复杂的组成,其中的罂粟碱的分子结构如图所示:已知该物质的燃烧产物为CO2、H2O和N2,1mol该化和物完全燃烧的耗氧量及在一定条件下与H2发生加成反应的耗氢量分别为( )
鸦片最早用于药物(有止痛、止泻、止渴作用),长期服用会成瘾,使人体质衰弱、精神颓废、寿命缩短.鸦片具有复杂的组成,其中的罂粟碱的分子结构如图所示:已知该物质的燃烧产物为CO2、H2O和N2,1mol该化和物完全燃烧的耗氧量及在一定条件下与H2发生加成反应的耗氢量分别为( )| A. | 26.5mol 8mol | B. | 23.25mol 8mol | C. | 23.25mol 10mol | D. | 26.5mol 6mol |
7.下列对沉淀溶解平衡的描述正确的是( )
| A. | 沉淀溶解达到平衡时,沉淀的速率和溶解的速率相等 | |
| B. | 电解质的溶解开始后,只有电解质的溶解过程,没有电解质的析出过程 | |
| C. | 沉淀溶解达到平衡时,溶液中溶质的各离子浓度相等,且保持不变 | |
| D. | 沉淀溶解达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解 |
8.如图是一氧化碳空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中,不正确的是( )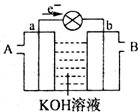

| A. | b电极上发生还原反应 | |
| B. | a电极的电极反应式为:CO+4OH-+2e-═CO32-+2H2O | |
| C. | B处通入的是空气 | |
| D. | 溶液中的K+向b电极方向移动 |