题目内容
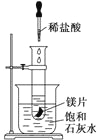
【题目】室温下,用某浓度NaOH溶液滴定一元酸HA的滴定曲线如图所示(横坐标为滴入NaOH的体积,纵坐标为所得混合液的pH).下列判断正确的是( ) 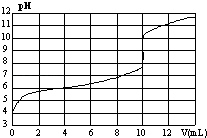
A.HA的浓度为1×10﹣4molL﹣1
B.实验时可选甲基橙作指示剂
C.pH=7时,溶液中c(Na+)>c(A﹣)
D.V=10mL,酸碱恰好中和
【答案】D
【解析】解:A.由图象分析可知,c(H+)=1×10﹣4molL﹣1 , 由于HA是弱酸,不完全电离,所以HA的浓度为大于1×10﹣4molL﹣1 , 故A错误;
B.氢氧化钠和弱酸反应恰好反应生成的盐是强碱弱酸盐,盐水解显碱性,应选择碱性条件下变色的指示剂,不能选择甲基橙,应选择酚酞指示剂,故B错误;
D.pH=7时,c(H+)=c(OH﹣),根据电荷守恒可知:c(Na+)=c(A﹣),故C错误;
D.由图象可知,当V=10mL曲线出现飞跃,说明酸碱恰好中和,故D正确;
故选D.

【题目】硒鼓回收料含硒约97%,其余为约3%的碲和微量的氯.从该回收料中回收硒的工艺流程如图所示(已知煅烧过程中,回收料中的硒、碲被氧化成SeO2和TeO2): 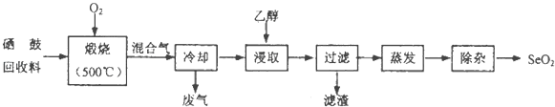
部分物质的物理性质如表:
物质 | 熔点 | 沸点 | 溶解度 |
SeO2 | 340℃(315℃升华) | 684℃ | 易溶于水和乙醇 |
TeO2 | 733℃(450℃升华) | 1260℃ | 微溶于水,不溶于乙醇 |
回答下列问题:
(1)Se与S是同族元素,比S多1个电子层,Se在元素周期表的位置为;H2Se的热稳定性比H2S的热稳定性(填“强”或“弱”).
(2)乙醇浸取后过滤所得滤渣的主要成分是 . 蒸发除去溶剂后,所得固体中仍含有少量TeO2杂质,除杂时适宜采用的方法是 .
(3)SeO2易溶于水得到H2SeO3溶液,向溶液中通入HI气体后,再加入淀粉溶液,溶液变蓝色,同时生成Se沉淀,写出反应的化学方程式 .
(4)已知H2SeO3的电离常数K1=3.5×10﹣3、K2=5.0×10﹣8 , 回答下列问题:
①Na2SeO3溶液呈性,原因是(用离子方程式表示);
②在Na2SeO3溶液中,下列关系式正确的是:
A.c(Na+)+c(H+)=c(SeO32﹣)+c(HSeO3﹣)+c(OH﹣)
B.2c(Na+)=c(SeO32﹣)+c(HSeO3﹣)+c(H2SeO3)
C.c(Na+)=2c(SeO32﹣)+2c(HSeO3﹣)+2c(H2SeO3)
D.c(OH﹣)=c(H+)+c(HSeO3﹣)+c(H2SeO3)