题目内容
13.从结构推测有机物CH2═CHCOOCH3最不可能具有的性质是( )| A. | 能发生取代反应 | B. | 能被新制Cu(OH)2悬浊液氧化 | ||
| C. | 能发生加聚反应 | D. | 能使溴水褪色 |
分析 分子中含有碳碳双键,可发生加成、加聚和氧化反应,含有酯基,可发生取代反应,以此解答该题.
解答 解:A.含有酯基,可发生取代反应,故A不选;
B.不含醛基,与氢氧化铜浊液不发生氧化还原反应,故B选;
C.含有碳碳双键,可发生加聚反应,故C不选;
D.含有碳碳双键,可与溴水发生加成反应,故D不选.
故选B.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,注意把握有机物的结构特点和官能团的性质,为解答该题的关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.下列有关化学现象及反应事实的解释中,方程式书写正确的是( )
| A. | 氢硫酸显弱酸性:H2S?2H++S2- | |
| B. | Na2CO3水溶液显弱碱性:CO32-+2H2O?H2CO3+2OH- | |
| C. | 用铜电极电解饱和NaCl溶液:阳极反应式是:2Cl--2e-=Cl2↑ | |
| D. | 用稀硝酸洗去试管中的银镜:3Ag+NO3-+4H+=3Ag++NO↑+2H2O |
18.关于摩尔质量的叙述正确的是( )
| A. | 氢气的摩尔质量是2克 | |
| B. | 1摩尔任何物质的质量通常叫做该物质的摩尔质量 | |
| C. | 1摩尔H2SO4的质量是98克/摩 | |
| D. | 氢气的摩尔质量是1g/mol |
5.下列实验操作:
①用50mL量筒量取5mL蒸馏水;
②称量没有腐蚀性固体药品时,把药品放在托盘上称量;
③浓硫酸沾到皮肤上要立即用大量水冲洗,并涂上稀硼酸;
④蒸馏时温度计的水银球应插在溶液中;
⑤分液漏斗分液时,上层液体应打开活塞从下口放出;
⑥固体药品用细口瓶保存.
其中错误的是( )
①用50mL量筒量取5mL蒸馏水;
②称量没有腐蚀性固体药品时,把药品放在托盘上称量;
③浓硫酸沾到皮肤上要立即用大量水冲洗,并涂上稀硼酸;
④蒸馏时温度计的水银球应插在溶液中;
⑤分液漏斗分液时,上层液体应打开活塞从下口放出;
⑥固体药品用细口瓶保存.
其中错误的是( )
| A. | ①②③ | B. | ③④ | C. | ②⑤⑥ | D. | 全部 |
2. 取x g NaHCO3和Na2O2的固体混合物放入一密闭容器中加热至250℃,充分反应后排出所有气体.将反应后的固体分成完全相同的两份,将其中一份投入到足量的BaCl2溶液中,最后可得到3.94g沉淀.另一份溶于适量的水,无气体放出,再向水溶液中缓缓加入盐酸,产生气体与所加盐酸体积之间的关系如图所示.
取x g NaHCO3和Na2O2的固体混合物放入一密闭容器中加热至250℃,充分反应后排出所有气体.将反应后的固体分成完全相同的两份,将其中一份投入到足量的BaCl2溶液中,最后可得到3.94g沉淀.另一份溶于适量的水,无气体放出,再向水溶液中缓缓加入盐酸,产生气体与所加盐酸体积之间的关系如图所示.
过氧化钠能发生的一些反应:2Na2O2+2H2O═4NaOH+O2↑;2Na2O2+2CO2═2NaCO3+O2↑;NaCO3+HCl═NaHCO3+NaCl;NaHCO3+HCl═NaCl+CO2↑+H2O.
试回答下列问题:
(1)加入盐酸后产生气体的在标准状况下的体积为0.448 L.
(2)将密闭容器中排出气体的化学式及对应的物质的量填入表格(有多少种填多少种)
(3)反应后的固体的成分(填化学式)NaOH、Na2CO3.
(4)x=6.09.
 取x g NaHCO3和Na2O2的固体混合物放入一密闭容器中加热至250℃,充分反应后排出所有气体.将反应后的固体分成完全相同的两份,将其中一份投入到足量的BaCl2溶液中,最后可得到3.94g沉淀.另一份溶于适量的水,无气体放出,再向水溶液中缓缓加入盐酸,产生气体与所加盐酸体积之间的关系如图所示.
取x g NaHCO3和Na2O2的固体混合物放入一密闭容器中加热至250℃,充分反应后排出所有气体.将反应后的固体分成完全相同的两份,将其中一份投入到足量的BaCl2溶液中,最后可得到3.94g沉淀.另一份溶于适量的水,无气体放出,再向水溶液中缓缓加入盐酸,产生气体与所加盐酸体积之间的关系如图所示.过氧化钠能发生的一些反应:2Na2O2+2H2O═4NaOH+O2↑;2Na2O2+2CO2═2NaCO3+O2↑;NaCO3+HCl═NaHCO3+NaCl;NaHCO3+HCl═NaCl+CO2↑+H2O.
试回答下列问题:
(1)加入盐酸后产生气体的在标准状况下的体积为0.448 L.
(2)将密闭容器中排出气体的化学式及对应的物质的量填入表格(有多少种填多少种)
| 化学式 | H2O | O2 | - |
| 物质的量(mol) | 0.05 | 0.00175 | - |
(4)x=6.09.
3.历史上最早应用的还原性染料--靛蓝,其结构简式如图所示,下列关于靛蓝的叙述中不正确的是( )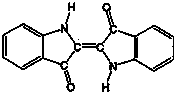

| A. | 靛蓝由碳、氢、氧、氮四种元素组成 | B. | 它的分子式是C16H10N2O2 | ||
| C. | 该物质是天然高分子化合物 | D. | 靛蓝中含苯环,属于芳香化合物 |
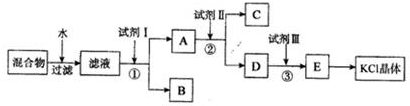
 如图所示的装置中,A是氯气发生装置,C、D为气体净化装置(C中装有饱和食盐水);D 中装有浓硫酸),E 是硬质玻璃管装有细铁丝网,F为干燥的空广口瓶,烧杯G 中装有氢氧化钠溶液.试回答:
如图所示的装置中,A是氯气发生装置,C、D为气体净化装置(C中装有饱和食盐水);D 中装有浓硫酸),E 是硬质玻璃管装有细铁丝网,F为干燥的空广口瓶,烧杯G 中装有氢氧化钠溶液.试回答: