题目内容
11.查尔酮类化合物有广泛的药理作用,下列反应是置于查尔酮类化合物的一种方法:
(1)化合物Ⅰ的分子式是C8H8O,1mol化合物Ⅰ完全燃烧能消耗7.5mol O2.
(2)下列关于化合物Ⅰ和化合物Ⅱ的说法正确的是BC.
A.化合物Ⅰ和化合物Ⅱ都能使溴的四氯化碳溶液褪色
B.用核磁共振氢谱可以区分化合物Ⅰ和化合物Ⅱ
C.含有苯环和醛基,与和化合物Ⅰ互为同分异构体的物质有4种
D.1mol化合物Ⅱ最多能与7mol H2发生加成反应.
分析 (1)由结构简式确定分子式为C8H8O,1mol化合物Ⅰ燃烧消耗氧气的物质的量为(6+$\frac{8}{4}$-$\frac{1}{2}$)mol;
(2)A.化合物Ⅰ不含碳碳双键,与溴不反应;
B.化合物Ⅰ和化合物Ⅱ都含有4种不同的H,且峰面积不同;
C.含有苯环和醛基,与和化合物Ⅰ互为同分异构体的物质,可为甲基苯甲醛(邻、间、对)以及苯乙醛等;
D.化合物Ⅱ含有3个苯环、1个碳碳双键,1个羰基,可发生加成反应;
解答 解:(1)由结构简式确定分子式为C8H8O,1mol化合物Ⅰ燃烧消耗氧气的物质的量为(6+$\frac{8}{4}$-$\frac{1}{2}$)mol=7.5mol,
故答案为:C8H8O;7.5;
(2)A.化合物Ⅰ不含碳碳双键,与溴不反应,故A错误;
B.化合物Ⅰ和化合物Ⅱ都含有4种不同的H,但峰面积不同,前者为1:2;2:3,后者为1:2:2:1,可鉴别,故B正确;
C.含有苯环和醛基,与和化合物Ⅰ互为同分异构体的物质,可为甲基苯甲醛(邻、间、对)以及苯乙醛等,共四种,故C正确;
D.化合物Ⅱ含有3个苯环、1个碳碳双键,1个羰基,可发生加成反应,则1mol化合物Ⅱ最多能与8mol H2发生加成反应.故D错误.
故选BC.
点评 本题考查有机物的结构和性质,题目综合考查学生分析问题能力和综合运用化学知识的能力,为高考常见题型,答题时注意把握题给信息以及有机物官能团的性质,为解答该题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 在Cl2与NaOH溶液的反应中,每0.1molCl2参加反应时,转移电子的数目为0.2NA | |
| B. | 0.1mol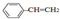 中含有双键的数目为0.4NA 中含有双键的数目为0.4NA | |
| C. | 标准状况下,11.2L乙醇中含有羟基的数目为0.5NA | |
| D. | 4.6g由NO2和N2O4组成的混合物中含有氧原子的数目为0.2NA |
2.某有机物的结构简式如图所示.下列关于该有机物的叙述错误的是( )


| A. | 分子式为C12H14O3 | B. | 分子中含有三种含氧官能团 | ||
| C. | 能够发生加成反应和取代反应 | D. | 可使溴水和酸性高锰酸钾溶液褪色 |
19.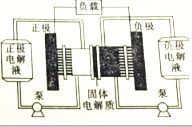 燃料电池实质上不能“储电”而是一个发电厂.某锂-铜空气燃料电池通过一种复杂的“铜腐蚀现象”产生电路,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法正确的是( )
燃料电池实质上不能“储电”而是一个发电厂.某锂-铜空气燃料电池通过一种复杂的“铜腐蚀现象”产生电路,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法正确的是( )
 燃料电池实质上不能“储电”而是一个发电厂.某锂-铜空气燃料电池通过一种复杂的“铜腐蚀现象”产生电路,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法正确的是( )
燃料电池实质上不能“储电”而是一个发电厂.某锂-铜空气燃料电池通过一种复杂的“铜腐蚀现象”产生电路,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法正确的是( )| A. | 该电池应该在负极通入空气 | |
| B. | 放电时,Li+透过固体电解质向负极移动 | |
| C. | 放电时,正极的电极反应式为Cu2O+2e-═2Cu+O2- | |
| D. | 整个反应过程中,铜相当于催化剂,氧化剂实质是O2 |
3.设NA 代表阿伏加德罗常数,下列说法不正确的是( )
| A. | 30g HCHO与过量的新制的氢氧化铜悬浊液反应转移了4NA个电子 | |
| B. | 1L 1mol/L 醋酸溶液中分子总数小于NA | |
| C. | 在1mol-CHO中所含电子数为15NA | |
| D. | 1mol CaHxNbOc的有机物中,H最多(2a+b+2)NA |
20.乙苯催化脱氢制苯乙烯反应:
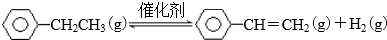
(1)已知:
计算上述反应的△H=+124 kJ•mol-1.
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸气发生催化脱氢反应.已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=$\frac{n{α}^{2}}{(1-{α}^{2})V}$(用α等符号表示).
(3)工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1:9),控制反应温度600℃,并保持体系总压为常压的条件下进行反应.在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图如下:
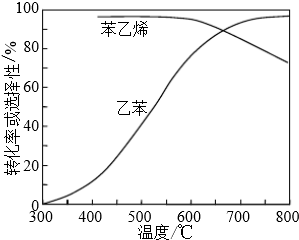
①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实正反应为气体分子数增大的反应,保持压强不变,加入水蒸气,容器体积应增大,等效为降低压强,平衡向正反应方向移动.
②控制反应温度为600℃的理由是600℃时乙苯的转化率与苯乙烯的选择性均较高,温度过低,反应速率较慢,转化率较低,温度过高,选择性下降,高温下可能失催化剂失去活性,且消耗能量较大.
(4)某研究机构用CO2代替水蒸气开发了绿色化学合成工艺----乙苯-二氧化碳耦合催化脱氢制苯乙烯.保持常压和原料气比例不变,与掺水蒸汽工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2═CO+H2O,CO2+C═2CO.新工艺的特点有①②③④(填编号).
①CO2与H2反应,使乙苯脱氢反应的化学平衡右移
②不用高温水蒸气,可降低能量消耗
③有利于减少积炭
④有利用CO2资源利用.
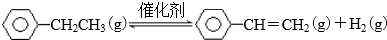
(1)已知:
| 化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ•molˉ1 | 412 | 348 | 612 | 436 |
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸气发生催化脱氢反应.已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=$\frac{n{α}^{2}}{(1-{α}^{2})V}$(用α等符号表示).
(3)工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1:9),控制反应温度600℃,并保持体系总压为常压的条件下进行反应.在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图如下:

①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实正反应为气体分子数增大的反应,保持压强不变,加入水蒸气,容器体积应增大,等效为降低压强,平衡向正反应方向移动.
②控制反应温度为600℃的理由是600℃时乙苯的转化率与苯乙烯的选择性均较高,温度过低,反应速率较慢,转化率较低,温度过高,选择性下降,高温下可能失催化剂失去活性,且消耗能量较大.
(4)某研究机构用CO2代替水蒸气开发了绿色化学合成工艺----乙苯-二氧化碳耦合催化脱氢制苯乙烯.保持常压和原料气比例不变,与掺水蒸汽工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2═CO+H2O,CO2+C═2CO.新工艺的特点有①②③④(填编号).
①CO2与H2反应,使乙苯脱氢反应的化学平衡右移
②不用高温水蒸气,可降低能量消耗
③有利于减少积炭
④有利用CO2资源利用.
1.下列指定反应的离子方程式正确的是( )
| A. | 氯气溶于水:Cl2+H2O=2H++Cl-+ClO- | |
| B. | Na2CO3溶液中CO32-的水解:CO32-+H2O=HCO3-+OH- | |
| C. | 酸性溶液中KIO3与KI反应生成I2:IO3-+I-+6H+=I2+3H2O | |
| D. | NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O |