题目内容
【题目】磷单质及其化合物有着广泛应用。
(1)在1.0 L密闭容器中放入0.10mol PCl5(g),一定温度进行如下反应:PCl5(g)![]() PCl3(g)+Cl2(g) ΔH1
PCl3(g)+Cl2(g) ΔH1
反应时间(t)与容器内气体总压强(p/100kPa)的数据见下表:
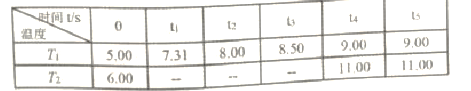
回答下列问题:
①PCl3的电子式为_______。
②T1温度下,反应平衡常数K=______。
③T1___T2(填“>”、“<”或“=”,下同),PCl5的平衡转化率α1(T1) __α2(T2)。
(2)PCl5、PCl3可转化为H3PO4、H3PO3。已知下列热化学方程式:
PCl5(g)+4H2O(l) = H3PO4(aq)+5HCl(aq) ΔH2
PCl3(g)+3H2O(l) = H3PO3(aq)+3HCl(aq) ΔH3
H3PO3(aq)+Cl2(g)+H2O(l) = H3PO4(aq)+2HCl(aq) ΔH4
则ΔH4= ______。(用ΔH1、ΔH2、ΔH3表示)
(3)次磷酸钴[Co(H2PO2)2]广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,原理如下图。
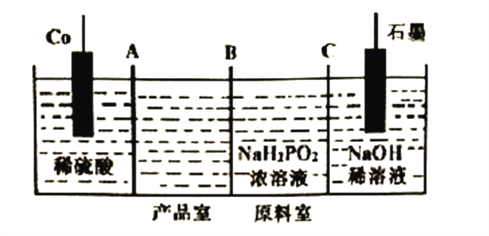
①Co的电极反应式为______________,A、B、C为离子交换膜,其中B为__________离子交换膜(填“阳”或“阴”)。
②次磷酸(H3PO2)为一元弱酸,次磷酸钠溶液中离子浓度由大到小的顺序是__________。
【答案】 ![]() 0.32 mol·L-1 < < ΔH2-ΔH1-ΔH3 Co-2e-=Co2+ 阴 c(Na+)>c(H2PO2-)>c(OH-)>c(H+)
0.32 mol·L-1 < < ΔH2-ΔH1-ΔH3 Co-2e-=Co2+ 阴 c(Na+)>c(H2PO2-)>c(OH-)>c(H+)
【解析】(1). ①.P原子最外层有5个电子,Cl原子最外层有7个电子,P原子与3个Cl原子形成3个共用电子对,PCl3的电子式为![]() ,故答案为:
,故答案为:![]() ;
;
②. 在恒温恒容的密闭容器中,容器内气体的总压强之比等于气体的总物质的量之比,根据平衡三段式法有:
PCl5(g)![]() PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
起始量(mol) 0.1 0 0
转化量(mol) x x x
平衡量(mol) 0.1-x x x
平衡时气体总物质的量为:(0.1-x+x+x)=(0.1+x)mol,则有:![]() =
= ![]() ,x=0.08mol,所以T1温度下,反应平衡常数K=
,x=0.08mol,所以T1温度下,反应平衡常数K=![]() =0.32 mol·L-1,故答案为:0.32 mol·L-1;
=0.32 mol·L-1,故答案为:0.32 mol·L-1;
③. 在1.0 L密闭容器中放入0.10mol PCl5(g),由表中数据可知,在时间为0时,T1对应的气体总压强小于T2对应的气体总压强,因相同条件下温度越高,气体的压强越大,所以T1<T2,在温度为T2时,根据平衡三段式法有:
PCl5(g)![]() PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
起始量(mol) 0.1 0 0
转化量(mol) y y y
平衡量(mol) 0.1-y y y
平衡时气体总物质的量为:(0.1-y+y+y)=(0.1+y)mol,则有:![]() =
= ![]() ,y=0.083mol,x=0.08mol<y=0.083mol,所以在温度为T2时PCl5的平衡转化率更大,即α1(T1) <α2(T2),故答案为:<;<;
,y=0.083mol,x=0.08mol<y=0.083mol,所以在温度为T2时PCl5的平衡转化率更大,即α1(T1) <α2(T2),故答案为:<;<;
(2). 已知:① PCl5(g)![]() PCl3(g)+Cl2(g) ΔH1、② PCl5(g)+4H2O(l) = H3PO4(aq)+5HCl(aq) ΔH2 ③ PCl3(g)+3H2O(l) = H3PO3(aq)+3HCl(aq) ΔH3,根据盖斯定律,②-①-③得H3PO3(aq)+Cl2(g)+H2O(l) = H3PO4(aq)+2HCl(aq),所以ΔH4=ΔH2-ΔH1-ΔH3,故答案为:ΔH2-ΔH1-ΔH3;
PCl3(g)+Cl2(g) ΔH1、② PCl5(g)+4H2O(l) = H3PO4(aq)+5HCl(aq) ΔH2 ③ PCl3(g)+3H2O(l) = H3PO3(aq)+3HCl(aq) ΔH3,根据盖斯定律,②-①-③得H3PO3(aq)+Cl2(g)+H2O(l) = H3PO4(aq)+2HCl(aq),所以ΔH4=ΔH2-ΔH1-ΔH3,故答案为:ΔH2-ΔH1-ΔH3;
(3). ①. 以金属钴和次磷酸钠为原料,用电解法制备次磷酸钴[Co(H2PO2)2],Co的化合价从0价升高到+2价,则Co的电极反应式为Co-2e-=Co2+,产品室可得到次磷酸钴的原因是:阳极室的Co2+通过阳离子交换膜进入产品室,原料室的H2
②. 次磷酸(H3PO2)为一元弱酸,在次磷酸钠溶液中,H2PO2-水解使溶液呈碱性,溶液中各离子浓度的大小关系为:c(Na+)>c(H2PO2-)>c(OH-)>c(H+),故答案为:c(Na+)>c(H2PO2-)>c(OH-)>c(H+)。

 全优点练单元计划系列答案
全优点练单元计划系列答案【题目】下列有关实验现象或事实解释正确的是( )。
选项 | 实验现象或事实 | 解释 |
A | 检验待测液中S | 先滴入盐酸可排除Ag+、C |
B | 制备乙酸乙酯时,导管应伸入试管至饱和Na2CO3溶液的液面上方 | 乙酸乙酯易溶于碳酸钠溶液,防止发生倒吸 |
C | 向Fe(NO3)2溶液中加入稀硫酸,试管口有红棕色气体产生 | 溶液中N |
D | 含Mg(HCO3)2的硬水长时间充分加热,最终得到的沉淀物的主要成分为Mg(OH)2,而不是MgCO3 | Ksp(MgCO3)<Ksp[Mg(OH)2] |
A. A B. B C. C D. D