题目内容
16.有6种无色液态物质:己烯、己烷、苯、甲苯、溴乙烷和乙醇,符合下列各题要求的分别是:(1)不能与溴水或酸性KMnO4溶液反应,但在铁屑作用下能与液溴反应的是苯,生成的有机物名称是溴苯,此反应属于取代反应.
(2)能与溴水发生反应的是己烯.
(3)能与酸性KMnO4溶液反应的是己烯、甲苯、乙醇.
(4)能与氢氧化钠水溶液反应的是溴乙烷,此反应属于取代反应.
(5)能发生消去反应的是溴乙烷、乙醇.
分析 不能与溴水或酸性KMnO4溶液反应的物质为己烷、苯,但苯易发生取代反应,如与液溴反应;而能与溴水或酸性KMnO4溶液反应的为己烯;不与溴水反应但与酸性KMnO4溶液反应为甲苯、乙醇等,溴乙烷、乙醇可发生消去反应,且溴乙烷可发生水解反应,以此来解答.
解答 解:(1)不能与溴水或酸性KMnO4溶液反应的物质为己烷、苯,但在铁屑作用下能与液溴反应的是苯,发生取代反应生成溴苯,故答案为:苯;溴苯;取代;
(2)己烯含有碳碳双键,可与溴水发生加成反应,故答案为:己烯;
(3)高锰酸钾具有强氧化性,可氧化己烯、甲苯、乙醇,故答案为:己烯、甲苯、乙醇;
(4)溴乙烷可在碱性条件下水解,为取代反应,故答案为:溴乙烷;取代;
(5)溴乙烷、乙醇可发生消去反应,其中溴乙烷在氢氧化钠醇溶液中发生消去反应,而乙醇在浓硫酸作用下发生消去反应,故答案为:溴乙烷、乙醇.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃及苯的同系物性质的考查,注意分析官能团,题目难度不大.

练习册系列答案
相关题目
6.某溶液中含K+、Al3+、NH4+、SO42-.取500mL该溶液加入过量的氢氧化钡溶液,经过滤、洗涤、干燥,称重得到9.32g固体1,并收集到224mL(标准状况)气体.在滤液中通入过量的CO2,经过滤、洗涤、灼烧,称重得到0.51g固体2.原溶液中K+的浓度为( )
| A. | 0.08mol/L | B. | 0.04mol/L | C. | 0.02mol/L | D. | 0.01mol/L |
7.V L含有(NH4)2SO4和K2SO4的混合溶液,已知NH4+浓度为a mol•L-1;SO42-浓度为bmol•L-1.则原混合溶液中钾离子的物质的量浓度为( )
| A. | (b-2a) mol•L-1 | B. | $\frac{b-2a}{2}$•L-1 | C. | (2b-a)mol•L-1 | D. | $\frac{2b-a}{2}$ mol•L-1 |
8.将下列各组物质按酸、碱、盐分类顺次排列,其中正确的是( )
| A. | 硫酸 纯碱 烧碱 | B. | 硝酸 烧碱 氯化钠 | ||
| C. | 醋酸 酒精 碳酸钙 | D. | 盐酸 熟石灰 苛性钠 |
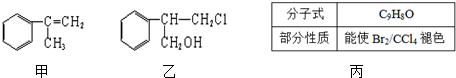
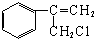 $→_{Ⅱ}^{一定条件}$Y$→_{Ⅲ}^{一定条件}$乙
$→_{Ⅱ}^{一定条件}$Y$→_{Ⅲ}^{一定条件}$乙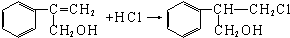 _(不需注明反应条件).
_(不需注明反应条件).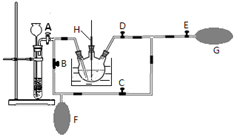 高锰酸钾是一种用途广泛的强氧化剂,实验室制备高锰酸钾所涉及的化学方程式如下:
高锰酸钾是一种用途广泛的强氧化剂,实验室制备高锰酸钾所涉及的化学方程式如下: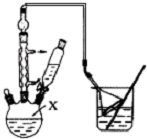 对叔丁基苯酚(
对叔丁基苯酚(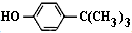 )工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等.实验室以苯酚、叔丁基氯等为原料制备对叔丁基苯酚.
)工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等.实验室以苯酚、叔丁基氯等为原料制备对叔丁基苯酚. .
.