题目内容
8. 过氧化氢是应用广泛的“绿色”氧化剂,酸性条件下稳定,中性或弱碱性条件下易分解.填空:
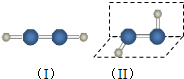
过氧化氢是应用广泛的“绿色”氧化剂,酸性条件下稳定,中性或弱碱性条件下易分解.填空:(1)过氧化氢的分子结构如图(Ⅱ),则过氧化氢属于极性(极性/非极性)分子.过去曾经有人认为过氧化氢的分子结构也可能是(Ⅰ),选择合理实验方法证明过氧化氢的分子结构为(Ⅱ)d(选填编号).
a.测定过氧化氢的沸点
b.测定过氧化氢分解时的吸收的能量
c.测定过氧化氢中H-O和O-O的键长
d.观察过氧化氢细流是否在电场中偏转
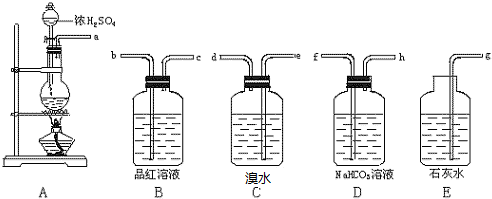
Na2O2,K2O2以及BaO2都可与酸作用生成过氧化氢.实验室可用稀硫酸和过氧化物在用冰冷却的条件下反应制取过氧化氢.
(2)上述过氧化物中最适合的是BaO2,反应完毕后过滤(填操作名称)即可得到双氧水.
(3)若反应时没有用冰冷却,会有气体产生,写出反应的化学方程式2BaO2+2H2SO4=2BaSO4+O2↑+2H2O.用酸性高锰酸钾溶液滴定双氧水的方法可以测定双氧水的浓度.
(4)取5.00mL 双氧水样品,配制成250mL溶液.此实验过程必须用到的两种主要仪器为酸式滴定管、250mL容量瓶(填仪器名称).
(5)取25.00mL上述溶液,用0.020mol/L的酸性高锰酸钾溶液滴定,看到溶液呈浅紫红色且半分钟内不褪色,到达滴定终点,消耗高锰酸钾溶液15.50mL.则原双氧水样品中含过氧化氢52.7 g/L.
分析 (1)由极性键构成的分子,若结构不对称,正负电荷中心不重叠则为极性分子;极性分子细液流在电场中会发生偏转;
(2)根据题目信息,实验室通过上述某种过氧化物与适量稀硫酸作用,过滤后即可制得较纯净的H2O2溶液,说明另一种产物为沉淀;
(3)BaO2与硫酸反应生成硫酸钡、氧气和水;
(4)双氧水具有强氧化性用酸式滴定管量取,配制250mL溶液需要250mL容量瓶;
(5)酸性高锰酸钾溶液为紫色,达到滴定终点时溶液呈浅紫红色且半分钟内不褪色;根据反应方程式计算25mL溶液中双氧水的物质的量,然后求出其质量,再求出1L溶液中的双氧水的质量.
解答 解:(1)H2O2分子中含有氧氢极性共价键和氧氧非极性共价键,由极性键构成的分子,若结构不对称,正负电荷中心不重叠则为极性分子;极性分子细液流在电场中会发生偏转;
a.分子的熔沸点与分子间作用力有关,与分子是否对称无关,故a错误;
b.过氧化氢分解时吸收的能量与氢氧键的键能有关,与分子是否对称无关,故b错误;
c.图示两种结构,过氧化氢分子中的氢氧键与氧氧键键长均相同,无法鉴别,故c错误;
d.图示两种结构,猜想1为对称结构的非极性分子,猜想2为非对称结构的极性分子,极性分子细液流在电场中发生偏转,非极性分子细液流在电场中不发生偏转,观察过氧化氢细液流在电场中是否发生偏转,可确定猜测中有一种正确,故d正确;
故答案为:极性;d;
(2)实验室通过上述某种过氧化物与适量稀硫酸作用,过滤后即可制得较纯净的H2O2溶液,说明另一种产物为沉淀,则生成了硫酸钡沉淀,所以选用BaO2;反应生成过氧化氢和硫酸钡沉淀,过滤即可得到纯净的过氧化氢;
故答案为:BaO2;过滤;
(3)若反应时没有用冰冷却,会有气体产生,则生成的氧气,即BaO2与硫酸反应生成硫酸钡、氧气和水,其反应的化学方程式为:2BaO2+2H2SO4=2BaSO4+O2↑+2H2O;
故答案为:2BaO2+2H2SO4=2BaSO4+O2↑+2H2O;
(4)双氧水具有强氧化性用酸式滴定管量取,配制250mL溶液需要250mL容量瓶,所以取5.00mL 双氧水样品,配制成250mL溶液,实验过程必须用到的两种主要仪器为酸式滴定管、250 mL容量瓶;
故答案为:酸式滴定管、250 mL容量瓶;
(5)酸性高锰酸钾溶液为紫色,达到滴定终点时双氧水完全反应,溶液变为浅紫红色且半分钟内不褪色;
反应离子方程式是:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O,
n(MnO4-)=cV=0.020mol/L×0.0155L=3.10×10-4mol,
n(H2O2)=$\frac{5}{2}$n(MnO4-)=$\frac{5}{2}$×3.10×10-4mol
则25.00mL上述溶液中双氧水的质量:m(H2O2)=nM=$\frac{5}{2}$×3.10×10-4mol×34g/mol=2.635×10-2g,
所以1000mL即1L双氧水样品溶液中双氧水的质量:m(H2O2)=2.635×10-2g×$\frac{1000mL}{5mL}$=52.7g,则则原双氧水样品中含过氧化氢52.7g/L,
故答案为:溶液呈浅紫红色且半分钟内不褪色;52.7.
点评 本题考查了制备实验方案设计,考查制备原理、分子结构、氧化还原反应的产物判断及方程式的书写、物质含量的计算等,难度中等,需要学生具备运用信息与基础知识分析问题、解决问题的能力.

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案| A. | 分子式为C10H14的一元取代芳烃,其可能的结构有5种 | |
| B. | 分子式为C2H4O的只能表示一种物质 | |
| C. | 甲酸甲酯能发生银镜反应,并与丙酸互为同系物 | |
| D. | 丙烯在一定条件下与水反应主要产物是2-丙醇 |
| A. | 金属性:Na<Mg<Al | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 酸性强弱:H2CO3<HSO4<HClO4 | D. | 熔点:Na>K>Rb |
| A. | 由于浓HNO3和浓H2SO4氧化性均较强,常温下都不可用铝制容器贮存 | |
| B. | 露置在空气中,容器内酸液的质量都减轻 | |
| C. | 常温下都能与铜较快反应 | |
| D. | 露置在空气中,容器内酸液的浓度都减小 |
| A. | 煤的干馏和煤的液化均是物理变化 | |
| B. | 海水淡化的方法有蒸馏法、电渗析法等 | |
| C. | 天然纤维和合成纤维的主要成分都是纤维素 | |
| D. | 用活性炭为糖浆脱色和用次氯酸盐漂白纸浆的原理相同 |
| A. | 淀粉、油脂、蛋白质都能水解,但水解产物不同 | |
| B. | 大豆富含蛋白质,故豆浆煮沸后蛋白质变成了氨基酸 | |
| C. | 石油的分馏、煤的气化、海水提溴的过程都包含化学变化 | |
| D. | 地淘油经处理后可作为汽车燃油,故地沟油的成分是液态烃 |