题目内容
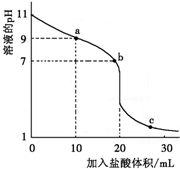 室温下,将0.100 0mol?L-1盐酸滴入20.00mL 未知浓度的某一元碱MOH溶液中,溶液pH随加入盐酸体积变化曲线如图所示.下列有关说法不正确的是( )
室温下,将0.100 0mol?L-1盐酸滴入20.00mL 未知浓度的某一元碱MOH溶液中,溶液pH随加入盐酸体积变化曲线如图所示.下列有关说法不正确的是( )分析:A.根据图象知,当盐酸体积为20mL时二者恰好反应生成盐,则二者的物质的量相等;
B.溶液的导电能力与离子浓度成正比;
C.常温下,MOH的电离常数Kb=
;
D.根据溶液酸碱性结合电荷守恒判断.
B.溶液的导电能力与离子浓度成正比;
C.常温下,MOH的电离常数Kb=
| c(M+).c(OH-) |
| c(MOH) |
D.根据溶液酸碱性结合电荷守恒判断.
解答:解:A.根据图象知,当盐酸体积为20mL时二者恰好反应生成盐,则二者的物质的量相等,二者的体积相等,则其浓度相等,所以一元碱溶液浓度为0.100 0 mol?L-1,故A正确;
B.溶液的导电能力与离子浓度成正比,MOH是弱电解质,HCl、MCl是强电解质,完全电离,根据图象知,a、b、c点的水溶液中,溶液中自由移动离子浓度逐渐增大,所以其导电性依次增强,故B正确;
C.根据图象知,0.1000mol/LMOH溶液中pH=11,则c(OHˉ)=0.001mol/L,常温下,MOH的电离常数Kb=
=
=1×10-5,故C正确;
D.b点溶液呈中性,则c(H+)=c(OHˉ),根据电荷守恒得c(M+)+c(H+)=c(OHˉ)+c(Clˉ),所以得c(M+)=c(Clˉ),故D错误;
故选D.
B.溶液的导电能力与离子浓度成正比,MOH是弱电解质,HCl、MCl是强电解质,完全电离,根据图象知,a、b、c点的水溶液中,溶液中自由移动离子浓度逐渐增大,所以其导电性依次增强,故B正确;
C.根据图象知,0.1000mol/LMOH溶液中pH=11,则c(OHˉ)=0.001mol/L,常温下,MOH的电离常数Kb=
| c(M+).c(OH-) |
| c(MOH) |
| (0.001)2 |
| 0.1000 |
D.b点溶液呈中性,则c(H+)=c(OHˉ),根据电荷守恒得c(M+)+c(H+)=c(OHˉ)+c(Clˉ),所以得c(M+)=c(Clˉ),故D错误;
故选D.
点评:本题考查了酸碱混合溶液定性判断,明确图象中各个点的含义是解本题关键,结合电荷守恒来分析解答,注意溶液的导电能力与离子浓度的关系,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
室温下,将0.1 mol下列物质分别加入蒸馏水中制成100 mL溶液,所得溶液中阴离子数目的大小顺序是①Na2O2 ②Na2O ③Na2CO3 ④Na2SO4
| A.①>②>③>④ | B.①>②>④>③ | C.①=②>③>④ | D.①=②>③=④ |

