题目内容
下列溶液中,物质的量浓度最小的是
| A.1 L H2SO4溶液中含98 g H2SO4 |
| B.0.5 L含49 g H2SO4的溶液 |
| C.98 g H2SO4溶于水配成2 L溶液 |
| D.0.1 L含24.5 g H2SO4的溶液 |
D
解析试题分析:A中C(H2SO4)=1mol/L.B中C(H2SO4)=(49g÷98g/mol)/0.5 L="1" mol/L.C中C(H2SO4)=(98g÷98g/mol)/2L=0.5mol/L. D.C(H2SO4)=(24.5g÷98g/mol)/0.1L=0.025mol/L.所以浓度最大的是选项D。
考点:考查物质的量浓度的有关计算的知识。

练习册系列答案
相关题目
下列所得溶液的物质的量浓度等于0.1 mol·L-1的是
| A.将0.1 mol氨气充分溶解在1 L水中 |
| B.将10g 1 mol·L-1的硫酸与90 g水混合 |
| C.将8g三氧化硫溶于水并配成1 L溶液 |
| D.将16g CuSO4·5H2O溶于水并配成1 L溶液 |
同温同压下,等质量的O2和O3相比较,下列结论正确的是( )
| A.它们的分子数目之比是 1∶1 | B.它们的氧原子数目之比为 2∶3 |
| C.它们的密度之比为 2∶3 | D.它们的体积之比是 1∶1 |
下列化学用语表示正确的是
A.Cl-离子的结构示意图: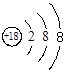 |
B.Ca(OH)2的电离方程式:Ca(OH)2 Ca2++2OH- Ca2++2OH- |
| C.稀盐酸中投入铁钉:2Fe+6HCl=2FeCl3+3H2↑ |
D.中子数为18的氯原子: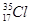 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,11.2LH2O含有的分子数为0.5NA |
| B.含有NA个氦原子的氦气在标准状况下的体积约为l1. 2L |
| C.25℃,l标准大气压下,64gSO2中含有的原子数为3NA |
| D.在常温常压下,11. 2LCl2含有的分子数为0.5NA |
设NA表示阿伏加德罗常数的值。下列说法正确的是
| A.0.1 mol Cl2完全溶于水,转移的电子数目为0.1NA |
| B.足量的硫单质与64g铜完全反应,转移电子数目为NA |
| C.1 mol Fe与足量的稀HNO3反应,转移2NA个电子 |
| D.含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol·L-1 |
下列说法中,正确的是( )。
| A.22.4 L N2含阿伏加德罗常数个氮分子 |
| B.在标准状况下,22.4 L水的质量约为18 g |
| C.22 g二氧化碳与标准状况下11.2 L HCl含有相同的分子数 |
| D.标准状况下,相同体积的任何气体单质所含的原子数相同 |
化学用语是学习化学的重要工具,下列化学用语中,正确的是
| A.硫酸与氢氧化钡中和:H+ + OH- = H2O |
B.碳酸氢钠的水解:HCO3-+ H2O  H3O++ CO32- H3O++ CO32- |
C.碳酸钠的水解:CO32-+2H2O  H2O+ CO2+2OH- H2O+ CO2+2OH- |
| D.氯化铝溶液中加入过量氨水:Al3+ + 3NH3·H2O = Al(OH)3↓+ 3 NH4+ |