题目内容
1.X、Y、Z三种元素都是短周期元素,在元素周期表中位置如图,X和Z原子核内的质子数之和等于Y原子核内质子数,下列推断正确的是( )| X | Z | |
| Y |
| A. | 原子半径:X>Y>Z | B. | 气态氢化物稳定性:X<Y<Z | ||
| C. | 元素的非金属性强弱:Y<X<Z | D. | Y和Z形成的是分子晶体 |
分析 X、Y、Z三种元素都是短周期元素,设X质子数为a,则Y、Z的质子数分别为a+8、a+2,X和Z原子核内的质子数之和等于Y原子核内质子数,则a+a+2=a+8,解得a=6,故X为C元素、Y为Si、Z为O元素.
A.同周期自左而右原子半径减小、同主族自上而下原子半径增大;
B.同周期自左而右原子非金属性增强、同主族自上而下非金属性减弱,非金属性越强,氢化物越稳定;
C.同周期自左而右原子非金属性增强、同主族自上而下非金属性减弱;
D.Si单质形成原子晶体.
解答 解:X、Y、Z三种元素都是短周期元素,设X质子数为a,则Y、Z的质子数分别为a+8、a+2,X和Z原子核内的质子数之和等于Y原子核内质子数,则a+a+2=a+8,解得a=6,故X为C元素、Y为Si、Z为O元素.
A.同周期自左而右原子半径减小、同主族自上而下原子半径增大,故原子半径:Y>X>Z,故A错误;
B.同周期自左而右原子非金属性增强、同主族自上而下非金属性减弱,非金属性越强,氢化物越稳定,故氢化物稳定性:Y<X<Z,故B错误;
C.同周期自左而右原子非金属性增强、同主族自上而下非金属性减弱,故非金属性:Y<X<Z,故C正确;
D.氧元素单质为分子晶体,但Si单质形成原子晶体,故D错误.
故选C.
点评 本题考查用结构性质位置关系应用,推断元素是解题关键,注意对元素周期律的理解掌握.

练习册系列答案
相关题目
1.下列关于元素周期表的构成说法正确的是( )
| A. | 有9个横行,分为7个周期 | B. | 有7个横行,分为7个周期 | ||
| C. | 有18个纵列,分为18个族 | D. | 有16个纵列,分为16个族 |
9.25℃,有v1mLpH≈9的氨水(A)和v2mLpH≈10的氨水(B),v3mLpH=10的NaOH溶液(C),它们能中和同量的盐酸,以下叙述正确的是( )
| A. | v1>10v2 | |
| B. | 加少量水稀释,氨水中$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$都减小 | |
| C. | v2≈v3 | |
| D. | 中和热A=B=C |
16.人类将在未来几十年内逐渐由“碳素燃料文明时代”过渡至“太阳能文明时代”(包括风能、生物质能等太阳能的转换形态),届时人们将适应“低碳经济”和“低碳生活”.下列说法不正确的是 ( )
| A. | 石油和天然气都属于碳素燃料 | |
| B. | 发展太阳能经济有助于减缓温室效应 | |
| C. | 太阳能电池可将太阳能转化为电能 | |
| D. | 目前研究菠菜蛋白质“发电”不属于“太阳能文明” |
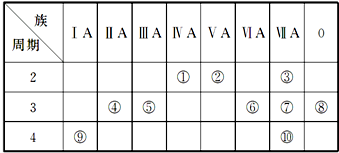
6.下表为元素周期表的一部分,列出10种元素在周期表中的位置.用化学符号回答下列问题:
(1)10种元素中,化学性质最活泼的金属是K.
(2)④、⑤、⑥三种元素最高价氧化物对应的水化物中,碱性最强的是NaOH.
(3)③、④三种元素形成的离子,离子半径由大到小的顺序是r(F-)>r(Na+).
(4)④和⑨两种元素形成化合物的化学式为NaBr,该化合物燃烧时的焰色为黄色,
该化合物溶液与元素⑧的单质反应的离子方程式为Cl2+2Br-=2Cl-+Br2.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑩ | ⑨ |
(2)④、⑤、⑥三种元素最高价氧化物对应的水化物中,碱性最强的是NaOH.
(3)③、④三种元素形成的离子,离子半径由大到小的顺序是r(F-)>r(Na+).
(4)④和⑨两种元素形成化合物的化学式为NaBr,该化合物燃烧时的焰色为黄色,
该化合物溶液与元素⑧的单质反应的离子方程式为Cl2+2Br-=2Cl-+Br2.
10.下列物质的分离和鉴别方法正确的是( )
| A. | 用分液法分离碘酒和CCl4 | |
| B. | 用饱和碳酸钠溶液萃取乙醇中的乙酸 | |
| C. | 用银氨溶液鉴别甲酸乙酯和乙醛 | |
| D. | 用浓溴水鉴别苯和环己烯 |
11.下列说法正确的是( )
| A. | 流水、风力是一次能源,电力、蒸汽是二次能源 | |
| B. | 普通锌锰电池是一次电池,碱性锌锰电池是二次电池 | |
| C. | 铅蓄电池是一次电池,氢氧燃料电池是二次电池 | |
| D. | 同周期元素形成的简单离子中,原子序数越大的离子半径越小 |
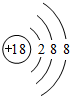 .
. ;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式):OH-、H3O+.
;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式):OH-、H3O+. Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀.
Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀.