题目内容
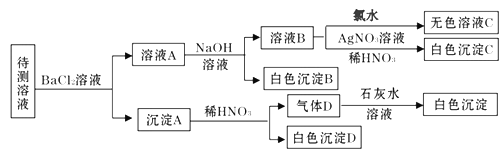
【题目】某待测溶液中可能含有Na+、SO42-、SO32-、Cl-、Br-、CO32-、HCO3-中的一种或多种,进行如下图所示的实验,每次实验所加试剂均过量。下列说法不正确的是
A. SO42-、SO32-至少含有一种
B. 沉淀B的化学式为 BaCO3
C. 肯定存在的离子有 Na+、CO32-、HCO3-、Cl-
D. 肯定不存在Br—
【答案】C
【解析】
待测液与氯化钡溶液反应生成沉淀A,则溶液中可能含有CO32-、SO42-、或SO32-,向沉淀A中加入稀硝酸生成气体D,气体D与石灰水作用产生白色沉淀,且有部分沉淀不溶解,则溶液中一定存在CO32-,可能存在SO42-、SO32-中的两种或一种;加入的氯化钡过量,所以溶液A中有Ba2+、Cl-,溶液A中加入过量的NaOH溶液得到白色沉淀B,则溶液中一定含有HC03-,白色沉淀B为BaCO3;溶液B中通入氯气,得无色溶液,溶液中一定不存在Br-;溶液B中加入硝酸酸化的硝酸银溶液得到白色沉淀,白色沉淀为AgCl,说明溶液B中含有C1-,由于开始时加入了氯化钡溶液,不能确定原溶液中是否含有Cl-。
A.根据以上分析可知,待测液中至少存在SO42-、SO32-中的一种,故A正确;B.根据分析可知,沉淀B为BaCO3,HCO3-与Ba2+、OH-反应生成的BaC03,故B正确;C.根据分析可知不能确定待测液中是否存在Cl-,故C错误;D.根据分析可知待测液中一定不存在Br-的离子,故D正确。答案:C。

【题目】氨是化学实验室及化工生产中的重要物质,应用广泛。
(1)已知25℃时:N2(g)+O2(g)![]() 2NO(g) ΔH=+183 kJ/mol
2NO(g) ΔH=+183 kJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ΔH=-1164.4 kJ/mol
则N2(g)+3H2(g)![]() 2NH3(g) ΔH=______kJ/mol
2NH3(g) ΔH=______kJ/mol
(2)在恒温恒容密闭容器中进行合成氨反应,起始投料时各物质浓度如下表:
N2 | H2 | NH3 | |
投料Ⅰ | 1.0 mol/L | 3.0 mol /L | 0 |
投料Ⅱ | 0.5 mol/L | 1.5 mol/L | 1.0 mol/L |
①按投料Ⅰ进行反应,测得达到化学平衡状态时H2的转化率为40%,则该温度下合成氨反应的平衡常数表达式为_______。
②按投料Ⅱ进行反应,起始时反应进行的方向为________(填“正向”或“逆向”)。
③若升高温度,则合成氨反应的化学平衡常数________(填“变大”、“变小”或“不变”)。
④L(L1、L2)、X可分别代表压强或温度。下图表示L一定时,合成氨反应中H2(g)的平衡转化率随X的变化关系。

ⅰ X代表的物理量是______。
ⅱ 判断L1、L2的大小关系,并简述理由______。
(3)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下:
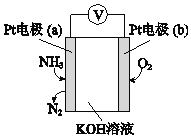
①电极b上发生的是______反应(填“氧化”或“还原”)。
②写出电极a的电极反应式_________。
【题目】某小组利用H2C2O4溶液和硫酸酸化的KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性KMnO4溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
实验编号 | 0.1mol/L酸性KMnO4溶液的体积/mL | 0.6mol/LH2C2O4溶液的体积/mL | H2O的体积/mL | 实验温度/℃ | 溶液褪色所需时间/min |
① | 10 | V1 | 35 | 25 | |
② | 10 | 10 | 30 | 25 | |
③ | 10 | 10 | V2 | 50 |
(1)表中V1=_______mL,V2=_______mL。
(2)探究温度对化学反应速率影响的实验编号是________(填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是________。
(3)实验①测得KMnO4溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H2C2O4)=________mol·L-1·min-1。