题目内容
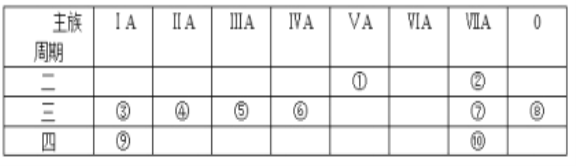
【题目】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在③~⑦元素中,原子半径最大的元素是________,其离子结构示意图为________
(2)元素的最高价氧化物对应的水化物中酸性最强的物质是________,碱性最强的物质是_______,呈两性的氢氧化物是________;
(3)按要求写出下列两种物质的电子式:①的氢化物________;⑨的最高价氧化物对应的水化物________;
(4)在⑦与⑩的单质中,化学性质较活泼的是_______,可用什么化学反应说明该事实(写出反应的化学方程式):_____________.
【答案】Na 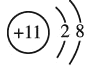 HClO4 KOH Al(OH)3
HClO4 KOH Al(OH)3 ![]()
![]() Cl2 2NaBr+Cl2=2NaCl+Br2
Cl2 2NaBr+Cl2=2NaCl+Br2
【解析】
根据元素的周期数和族序数,可以判断①是N,②是F,③是Na,④是Mg,⑤是Al,⑥是Si,⑦是Cl,⑧是Ar,⑨是K,⑩是Br。
(1)同周期元素从左到右,原子半径逐渐减小,在③~⑦元素中,原子半径最大的是Na;其离子为Na+,与钠原子比较少了一个电子,Na+的结构示意图为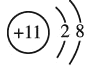 ;
;
(2)周期表中,从上到下,元素的最高价氧化物对应水化物的碱性逐渐增强,酸性逐渐减弱,从左到右,元素的最高价氧化物对应水化物的酸性逐渐增强,碱性逐渐减弱,在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的物质是KOH,呈两性的氢氧化物是Al(OH)3;
(3)①的氢化物NH3,电子式为![]() ;⑨的最高价氧化物的对应的水化物是KOH,钾离子电子式K+,氢氧根电子式为
;⑨的最高价氧化物的对应的水化物是KOH,钾离子电子式K+,氢氧根电子式为![]() ,KOH的电子式为
,KOH的电子式为![]() ;
;
(4)同主族元素,从上到下,单质的氧化性逐渐减弱,所以在氯气和溴的单质中,化学性质较为活泼的是氯气,因为氯气可以与溴化钾反应,置换出单质溴,答案:Cl2,2NaBr+Cl2=2NaCl+Br2。

【题目】某课题组为了深入探究二氧化硫的性质设计以下装置进行了实验。

步骤一:检验装置气密性后向B、C中各加入20mL图示液体。
步骤二:打开A中活塞,反应进行10分钟后关闭活塞。
步骤三:用pH计分别测量B、C试管中溶液的pH。
结合上述实验,回答以下问题:
请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是________,其中发生反应的化学方程式为_______________________。
(2)甲同学认为两瓶中pH大致相等,原因是二氧化硫溶于水后生成了酸性物质_____________,该物质发生电离所致。
(3)通过pH计测定,B瓶中pH为2.13,C瓶中pH为1.05。为了解释该实验现象,该同学提出进行多次平行实验,目的是_______________________。
测定结果如下:
第1次实验 | 第2次实验 | 第3次实验 | |
B瓶中pH | 2.15 | 2.10 | 2.17 |
C瓶中pH | 1.10 | 1.12 | 1.09 |
实验发现:C瓶中溶液的酸性始终比B瓶中的酸性强。
(4)通过查阅文献,I﹣可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程分两步进行如下,将ii补充完整。
i.SO2+4I﹣+4H+=S↓+2I2+2H2O
ii.I2+2H2O+___═___+___+2I﹣
(5)最终结论:C瓶中溶液酸性强于B瓶,是由于生成了____________,该过程中体现出二氧化硫哪些化学性质________________(选填“氧化性”,“还原性”)。