题目内容
在恒容密闭容器中,可逆反应H2(g)+I2(g)  2HI(g) 达到平衡状态时的标志是
2HI(g) 达到平衡状态时的标志是
| A.混合气体的体积恒定不变 |
| B.混合气体的颜色不再改变 |
| C.H2、I2、HI的浓度相等 |
| D.I2在混合气体中的体积分数与H2在混合气体中的体积分数相等 |
B
解析试题分析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。颜色的深浅和浓度有关系,所以选项B可以说明。反应前后气体的体积不变,因此气体的总物质的量、体积和压强始终是不变的,A不能说明。平衡时各种物质的浓度不再发生变化,但各种的浓度之间不一定满足某种关系,CD不能说明,因此答案选A。
考点:考查可逆反应平衡状态的判断
点评:该题是中等难度的试题,也是高考中的常见题型和考点。试题基础性强,难易适中,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确平衡状态的特点,然后结合具体的可逆反应灵活运用即可。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
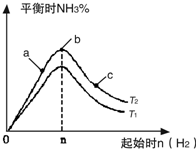 利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题: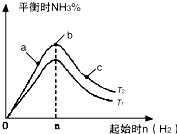 利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题: