题目内容
20.过氧化钙可以用于改善地表水质、处理含重金属粒子废水和治理赤潮,也可用于应急供氧等.工业上生产过氧化钙的主要流程如图: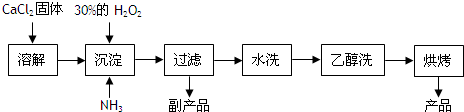
已知CaO2•8H2O呈白色,微溶于水,加热至350℃左右开始分解放出氧气.
(1)用上述方法制取CaO2•8H2O的化学方程式是CaCl2+H2O2+2NH3+8H2O=CaO2•8H2O↓+2NH4Cl;
(2)检验“水洗”是否合格的方法是取最后一次洗涤液少许于试管中,再滴加稀硝酸酸化的硝酸银溶液,看是否产生白色沉淀;
(3)沉淀时常用冰水控制温度在0℃左右,其可能原因是(写出两种):
①温度低可减少过氧化氢的分解,提高过氧化氢的利用率
②该反应是放热反应,温度低有利于提高CaO2•8H2O产率
(4)测定产品中CaO2的含量的实验步骤是:
第一步:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2mol/L的H2SO4溶液,充分反应.
第二步:向上述锥形瓶中加入几滴淀粉溶液.
第三步:逐滴加入浓度为c mol•L-1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液V mL.
【已知:I2+2S2O32-═2I-+S4O62-】
①CaO2的质量分数为$\frac{36cV×1{0}^{-3}}{a}$或$\frac{3.6cV}{a}$ (用字母表示);
②某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能偏高(填“不受影响”、“偏低”或“偏高”),原因是在酸性条件下空气中的O2也可以把KI氧化为I2,使消耗的Na2S2O3增多,从而使测得的CaO2的质量分数偏高.
分析 (1)根据图示流程中找出反应物、生成物,写出反应的化学方程式,由工艺流程可知,反应②为氯化钙与氨水、过氧化氢反应生成CaO2•8H2O,还应生成氯化铵;
(2)通过检验洗涤液中是否含有氯离子来判断检验“水洗”是否合格,用稀硝酸酸化的硝酸银溶液检验;
(3)从双氧水的稳定性、该反应的反应热、温度对过氧化钙的溶解度的影响等方面分析;
(4)①根据电子守恒及化学反应方程式找出过氧化钙与硫代硫酸钠反应的关系式,再根据题中数据计算出样品中过氧化钙的质量分数;
②根据空气中的氧气能够氧化碘离子,使碘单质的量增加,消耗的硫代硫酸钠增加分析.
解答 解:(1)由流程可知,反应物为氯化钙、双氧水、氨气和水,生成为CaO2•8H2O和氯化铵,反应的化学方程式为:CaCl2+H2O2+2NH3+8H2O=CaO2•8H2O↓+2NH4Cl,
故答案为:CaCl2+H2O2+2NH3+8H2O=CaO2•8H2O↓+2NH4Cl;
(2)“水洗”不合格,含有氯离子,所以检验“水洗”是否合格的方法是:取最后一次洗涤液少许于试管中,再滴加稀硝酸酸化的硝酸银溶液,看是否产生白色沉淀,
故答案为:取最后一次洗涤液少许于试管中,再滴加稀硝酸酸化的硝酸银溶液,看是否产生白色沉淀;
(3)由于温度较高时双氧水容易分解,会导致过氧化钙产率下降,且温度降低时过氧化钙的溶解度减小,有利于过氧化钙的析出,该反应是放热反应,温度低有利于提高CaO2•8H2O产率,所以沉淀反应时常用冰水浴控制温度在0℃左右,
故答案为:温度低可减少过氧化氢的分解,提高过氧化氢的利用率;该反应是放热反应,温度低有利于提高CaO2•8H2O产率;
(4)①过氧化钙氧化碘化钾生成的碘单质,用硫代硫酸钠滴定时,消耗的硫代硫酸钠的物质的量为:cmol•L-1×V×10-3L=cV×10-3mol,根据氧化还原反应中电子守恒及题中反应方程式可得关系式:CaO2~I2~2S2O32-,过氧化钙的物质的量为:n(CaO2)=$\frac{1}{2}$n(S2O32-)=$\frac{1}{2}$×cV×10-3mol,
样品中CaO2的质量分数为:$\frac{\frac{1}{2}×cV×1{0}^{-3}mol×72g/mol}{ag}$×100%=$\frac{36cV×1{0}^{-3}}{a}$或$\frac{3.6cV}{a}$,
故答案为:$\frac{36cV×1{0}^{-3}}{a}$或$\frac{3.6cV}{a}$;
③在酸性条件下空气中的O2也可以把KI氧化为I2,使消耗的Na2S2O3增多,从而使测得的CaO2的质量分数偏高,
故答案为:偏高;在酸性条件下空气中的O2也可以把KI氧化为I2,使消耗的Na2S2O3增多,从而使测得的CaO2的质量分数偏高.
点评 本题考查形式为物质制备流程图题目,涉及中和滴定中的误差分析、物质的检验及化学计算等问题,题目难度较大,做题时注意分析题中关键信息、明确实验基本操作方法,本题较为综合,充分考查了学生的分析、理解能力及化学实验、化学计算能力.

| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 | SO42- HCO3-NO3- OH- |
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,仅有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,只有A中放出无色气体,只有C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)写出B、D的化学式:BKNO3,DCuSO4.
(2)在A溶液中加入少量澄清石灰水,观察到的现象为产生白色沉淀
(3)将含lmol A的溶液与含l mol E的溶液反应后蒸干,仅得到一种化合物,该化合物化学式为Na2CO3.反应的离子方程式是HCO3-+OH-=H2O+CO32-.
(4)C常用作净水剂,用离子方程式表示其净水原理Al3++3H2O?Al(OH)3(胶体)+3H+.
| A. | 向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42-═BaS04↓+2H2O | |
| B. | 酸性介质中KMnO4氧化 H2O2:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O | |
| C. | 等物质的量的MgCl2、Ba(OH)2 和 HCl 溶液混合:Mg2++2OH-═Mg(OH)2↓ | |
| D. | 铅酸蓄电池充电时的正极反应:PbSO4+2H2O-2e-═PbO2+4H++SO42- |
| A. | 将SO3分离出一部分 | B. | 升温 | ||
| C. | 充入少量N2,增大压强 | D. | 充入少量SO3气体 |
| A. | ③①②④⑤ | B. | ③①⑤②④ | C. | ③⑤②①④ | D. | ③①②⑤④ |
 如图所示物质的转化关系中,A是一种固体单质,E是一种白色沉淀.请回答下列问题:
如图所示物质的转化关系中,A是一种固体单质,E是一种白色沉淀.请回答下列问题: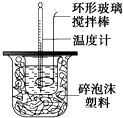 在量热器中将50ml、0.50mol•L-1CH3COOH溶液与50ml、0.55mol•L-1NaOH溶液混合,温度从25.160C升高到27.460C.已知量热计的热容常数(量热计各部件每升高10C所需的热量)是150J•0C-1,C=4.18J•g-1•0C-1,溶液的密度为1g•cm-3.
在量热器中将50ml、0.50mol•L-1CH3COOH溶液与50ml、0.55mol•L-1NaOH溶液混合,温度从25.160C升高到27.460C.已知量热计的热容常数(量热计各部件每升高10C所需的热量)是150J•0C-1,C=4.18J•g-1•0C-1,溶液的密度为1g•cm-3.