��Ŀ����
����Ŀ����ijͬѧΪ̽��Ԫ�����ڱ���ͬ����Ԫ�����ʵĵݱ���ɣ����������ϵ��ʵ�飮
��1�����ơ�þ������1mol�ֱ�Ͷ�뵽������ͬŨ�ȵ������У���Ԥ��ʵ�����������ᷴӦ����ң������ᷴӦ������������࣮
��2����Na2S��Һ��ͨ���������ֻ�ɫ���ǣ���֤��Cl�ķǽ����Ա�Sǿ����Ӧ�����ӷ���ʽΪ ��
��3�������D�������� ��
��4����Ҫ֤���ǽ����ԣ�Cl��I����A�м�Ũ���ᣬB�м�KMnO4 �� ��KMnO4��Ũ���᳣���·�Ӧ������������C�мӵ��۵⻯�ػ����Һ���۲쵽C����Һ��������֤�����ӻ��������Ĺ۵㿼�ǣ���װ��ȱ��β������װ�ã�������Һ����β����
��5����Ҫ֤���ǽ����ԣ�C��Si������A�м����ᡢB�м�CaCO3��C�м�Na2SiO3��Һ���۲쵽C����Һ��������֤�������е�ͬѧ��Ϊ������лӷ��ԣ��ɽ���C�и���ʵ�飬Ӧ����װ�ü�����װ����Һ��ϴ��ƿ�� 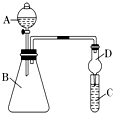
���𰸡�
��1���ƣ���
��2��S2��+Cl2�TS��+2Cl����������ͼװ�ÿ���֤ͬ����Ԫ�طǽ����Եı仯����
��3����ֹ��Һ����
��4��������NaOH
��5���а�ɫ�������ɣ�����NaHCO3
���������⣺��1��ͬ���ڴ������ң�����ԭ�������ĵ�����Ԫ�صĽ������������ơ�þ��������ͬһ���ڣ���ԭ��������������ݽ������˳�������������˳���֪�����������ԣ��ƣ�þ������������ͬ�����������ᷴӦ��ҵ����ƣ���Ӧ��������������������1mol������Ҫ�õ�2mol���ӣ�1mol�ƶ�ʧȥ1mol���ӣ�1molþʧȥ2mol���ӣ���1mol��ʧȥ3mol���ӣ������������������ǽ����������Դ��ǣ��ƣ����� ��2������������ǿ�����ʣ����������ܹ��������ӷ�Ӧ������Ӧ�����ӷ���ʽΪ��S2��+Cl2�TS��+2Cl�� �� ���Դ��ǣ�S2��+Cl2�TS��+2Cl�� �� ��3�����θ����D���β��־��нϴ�ռ䣬�������ã��ܹ���ֹ���������Ա���C��Һ�������ƿ�У� ���Դ��ǣ���ֹ��Һ��������4��KMnO4��Ũ���ᷴӦ����������2KMnO4+16HCl�T2KCl+2MnCl2+5Cl2��+8H2O����������۵⻯�ػ����Һ��Ӧ���ɵⵥ�ʣ���Ӧ���ӷ���ʽΪ��2I��+Cl2�TI2+2Cl�� �� ����������Һ����ɫ����C����Һ��Ϊ��ɫ����������������ɢ�������У���Ⱦ����������NaOH��Һ���գ���Ӧ���ӷ���ʽΪ��2OH��+Cl2�TCl��+ClO��+H2O�����Դ��ǣ�������NaOH����5����̼��ȹ���ǿ��������̼��������Ʒ�Ӧ���ɹ����������Һ����ǣ��Ȼ�����лӷ��ԣ�����ʵ��������Ҫ��������̼�е��Ȼ�������������Ȼ�����̼�����Ʒ�Ӧ����������̼����Ӧ��������B��C֮������װ�б���NaHCO3��Һ��ϴ��ƿ�����Դ��ǣ��а�ɫ�������ɣ�����NaHCO3��Һ��

 �ŵ������ϵ�д�
�ŵ������ϵ�д�
