题目内容
【题目】下列物质分离的方法正确的是( )
A.从碘水中提取碘:用酒精萃取
B.除去CO中少量O2:通过灼热的Cu网后收集气体
C.除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤
D.除去CO2中的少量HCl:通入饱和NaHCO3溶液,收集气体
【答案】D
【解析】A.酒精与水混溶,应用苯或四氯化碳作萃取剂,A不符合题意;
B.CO被氧化生成二氧化碳,应用灼热的碳,B不符合题意;
C.加入氢氧化钠,生成氯化钠,引入新杂质,应加入氢氧化钾,C不符合题意;
D.二氧化碳与饱和碳酸氢钠不反应,且难溶于饱和碳酸氢钠,可用于除杂,D符合题意;
所以答案是:D.

【题目】以含钴废催化剂(主要成分为Co、Fe、SiO2)为原料制取复合氧化钴的流程如下:
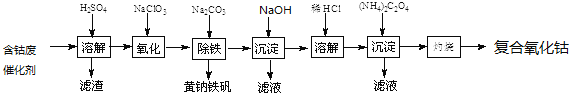
(1)用H2SO4溶解后过滤,得到的滤渣是_________(填化学式)。将滤渣洗涤2~3次,再将洗液与滤液合并的目的是____________________。
(2)在加热搅拌条件下加入NaClO3,将Fe2+氧化成Fe3+,反应的离子方程式是___________________。
(3)已知:铁氰化钾的化学式为K3[Fe(CN)6];亚铁氰化钾的化学式为K4[Fe(CN)6]。
3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓(蓝色沉淀)
4Fe3++3[Fe(CN)6]4-=Fe4[Fe(CN)6]3↓(蓝色沉淀)
确定Fe2+是否氧化完全的方法是__________________。(仅供选择的试剂:铁氰化钾溶液、亚铁氰化钾溶液铁粉、KSCN溶液)
(4)向氧化后的溶液中加入适量的Na2CO3调节酸度,使之生成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,写出该反应的离子方程式:_______________________。
(5)弱酸和弱碱的电离平衡常数的负对数可用pK表示,根据下表中数据判断(NH4)2C2O4溶液中各离子的浓度由大到小的顺序为__________________。
H2C2O4 | pKa1= l.25,pKa2=4.13 |
NH3·H2O | pKb=4.76 |
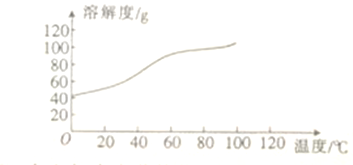
(6)已知CoCl2的溶解度曲线如图所示。向碱式碳酸钴中加入足量稀盐酸边加热边搅拌至完全溶解后,需趁热过滤其原因是_____________________。
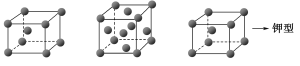
(7)准确称取1.470gCoC2O4,在空气中充分灼烧得0.814g复合氧化钴,写出复合氧化钴的化学式:_________________________。