题目内容
4.在托盘天平左右两边分别放上等质量的足量的水和稀H2SO4,指针位于中心,向左烧杯中投入一定量的金属Na(2Na+2H2O═2NaOH+H2↑),右烧杯中投入一定量的金属Mg,充分反应后发现指针仍位于中心,则左盘和右盘转移的电子数之比为( )| A. | 1:2 | B. | 1:1 | C. | 2:1 | D. | 不能确定 |
分析 加入Na和Mg后,充分反应后发现指针仍位于中心,说明溶液增加的质量相同,结合方程式计算出Na、Mg的质量,再求出物质的量和转移电子.
解答 解:设向左烧杯中投入的金属Na为xg,右烧杯中投入的金属Mg为yg,令溶液增加的质量为mg;
2Na+2H2O═2NaOH+H2↑△m
46 46-2
xg mg
Mg+H2SO4═MgSO4+H2↑△m
24 24-2
yg mg
则x=$\frac{46m}{44}$=$\frac{23m}{22}$,y=$\frac{24m}{22}$=$\frac{12m}{11}$,
所以左盘和右盘转移的电子数之比为$\frac{\frac{23m}{22}}{23}$×1:$\frac{\frac{12m}{11}}{24}$×2=1:2;
故选A.
点评 本题考查了有关方程式的计算,题目难度中等,侧重于考查学生的分析能力和计算能力,注意根据溶液的质量变化结合方程式分析.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
14.下列实验操作符合安全要求的是( )
| A. | 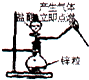 | B. |  | C. |  | D. |  |
15.下列说法中不正确的是( )
| A. | 在燃煤中加入石灰石可减少SO2排放,发生的反应为2CaCO3+2SO2+O22CO2+2CaSO4 | |
| B. | CO2通入水玻璃可以得到硅酸沉淀 Na2SiO3+CO2+H2O═Na2CO3+H2SiO3↓ | |
| C. | 硅主要以单质、氧化物、硅酸盐的形式存在于自然界中 | |
| D. | 氢氟酸能够雕刻玻璃,故不能用玻璃瓶在盛装氢氟酸 SiO2+4HF═SiF4↑+2H2O |
19.下列关于生活中的现象及仪器的使用的说法不正确的是( )
| A. | “酸可除锈”、“纯碱溶液可去油污”都发生了化学变化 | |
| B. | 被蜂蚁蜇咬会感到疼痛难忍,这是蜂蚁咬人时将甲酸注入人体的缘故,此时若能涂抹稀氨水或碳酸氢钠溶液,可以减轻疼痛 | |
| C. | 托盘天平称量药品时,都应垫上滤纸称量 | |
| D. | 滴定管以及容量瓶在使用前需检查是否漏水 |
7.已知:25℃时,Ksp[Mg(OH)2]=5.61×10-12,Ksp(MgF2)=7.42×10-11.下列说法正确的是( )
| A. | 25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大 | |
| B. | 25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大 | |
| C. | 25℃时,Mg(OH)2固体在20 mL 0.01 mol/L氨水中的Ksp比在20 mL 0.01 mol/L NH4Cl溶液中的Ksp小 | |
| D. | 25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2不可能转化成为MgF2 |