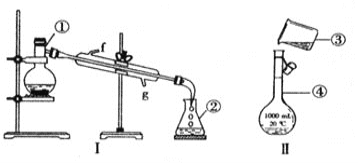
题目内容
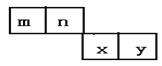
【题目】m、n、x、y四种主族元素在周期表的相对位置如图所示。已知它们的原子序数总和为46,则:
(1)元素n的气态氢化物的电子式为___,基态n原子的核外共有__种不同运动状态的电子。
(2)m与y所形成的化合物含___键,属___分子。(填“极性”或“非极性”)
(3)x位于周期表的第___周期第___族;其简单离子的离子结构示意图为___。
【答案】![]() 7 极性 非极性 三 VIA
7 极性 非极性 三 VIA 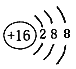
【解析】
设m的原子序数是a,根据m、n、x、y四种主族元素在周期表的相对位置,n、x、y的原子序数是a+1、a+10、a+11,a+a+1+a+10+a+11=46,a=6,所以m、n、x、y四种主族元素分别是C、N、S、Cl。
(1) n是N元素,N的气态氢化物是NH3,电子式为![]() ,核外电子的运动状态都不同,基态N原子的核外共有7个电子,所以有7种不同运动状态的电子。
,核外电子的运动状态都不同,基态N原子的核外共有7个电子,所以有7种不同运动状态的电子。
(2)C与Cl所形成的化合物是CCl4,含极性共价键,CCl4分子结构对称,属非极性分子;
(3)S元素位于周期表的第三周期第VIA族;其简单离子S2-的核外有18个电子,离子结构示意图为 。
。

【题目】部分难溶物的颜色和常温下的Ksp如下表所示:
Cu(OH)2 | CuOH | CuCl | Cu2O | |
颜色 | 蓝色 | 黄色 | 白色 | 砖红色 |
Ksp(25 ℃) | 1.6×10-19 | 1.0×10-14 | 1.2×10-6 | — |
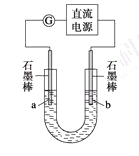
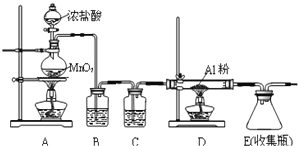
某研究性学习小组对电解食盐水进行了如下探究:
实验Ⅰ装置如图所示,接通电源后,发现a、b电极上均有气泡产生。
(1)电解过程中的总离子反应方程式为_________________________________________。
(2)为了确定电源的正、负极,下列操作一定行之有效的是_______。
A.观察两极产生气体的颜色
B.往U形管两端分别滴入数滴酚酞试液
C.用燃着的木条靠近U形管口
D.在U形管口置一张湿润的淀粉KI试纸
实验Ⅱ把上述电解装置的石墨棒换成铜棒,用直流电源进行电解,装置如图所示。
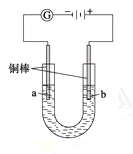
观察到的现象如下所示:
①开始无明显现象,随后液面以下的铜棒表面逐渐变暗;
②5 min后,b极附近开始出现白色沉淀,并逐渐增多,且向a极扩散;
③10 min后,最靠近a极的白色沉淀开始变成红色;
④12 min后,b极附近的白色沉淀开始变成黄色,然后逐渐变成橙黄色;
⑤a极一直有大量气泡产生;
⑥停止电解,将U形管中悬浊液静置一段时间后,上层溶液呈无色,没有出现蓝色,下层沉淀全部显砖红色。
(3) a极发生的电极反应方程式为________________________________________________________。
(4) 电解5 min后,b极发生的电极反应方程式为___________________________________________。
(5)12 min后,b极附近出现的橙黄色沉淀的成分是_____,原因是___________________________________________________________________________________。