题目内容
已知:2M(g) N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器
N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器
中,反应体系中物质浓度随时间变化关系如右图所示。下列说法正确的是( )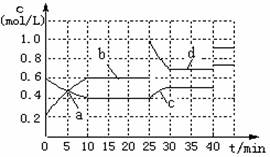
| A.a、b、c、d四个点中处于平衡状态的点是a、b |
| B.反应进行至25min时,曲线发生变化的原因是加入了 0.4molN |
| C.若调节温度使35min时体系内N的百分含量与15min时相等,应升高温度 |
| D.若40min后出现如图所示变化,则可能是加入了某种催化剂 |
C
解析试题分析:A.当可逆反应达到化学平衡时平衡混合物的浓度都保持不变。在上述四点中处于平衡状态的点是b、d.错误。B. B.反应进行至25min时,M的浓度突然增加0.4mol/L,而N的浓度在这一瞬间没变化,曲线发生变化的原因是加入了 0.4molM。错误。C.该反应的正反应是放热反应。当可逆反应达到化学平衡时,升高温度,化学平衡向吸热方向移动。即对于该反应来说向逆反应方向移动。所以N的含量降低到15min时相等。正确。D.加入了某种催化剂不能使化学平衡发生移动。个物质的浓度都不变。错误。
考点:考查化学平衡状态的判断及外界条件对化学平衡的影响的知识。

 阅读快车系列答案
阅读快车系列答案已知:H2(g) +I2(g)  2HI(g) ΔH =" -14.9" kJ/mol。在甲、乙两个体积相同密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)="0.008" mol/L。 下列判断正确的
2HI(g) ΔH =" -14.9" kJ/mol。在甲、乙两个体积相同密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)="0.008" mol/L。 下列判断正确的
| 起始浓度 | c(H2) / mol/L | c(I2) / mol/L | c(HI) / mol/L |
| 甲 | 0.01 | 0.01 | 0 |
| 乙 | 0.02 | 0.02 | 0 |
A.平衡时,乙中H2的转化率是甲中的2倍
B.平衡时,甲中混合物的颜色比乙中深
C.平衡时,甲、乙中热量的变化值相等
D.该温度下,反应的平衡常数K=0.25
对于某一可逆反应,改变下列条件,一定能使化学平衡发生移动的是( )
| A.增加某反应物的质量 | B.使用催化剂 |
| C.降低反应体系的压强 | D.升高温度 |
在水溶液中,重铬酸钾K2Cr2O7存在以下平衡: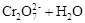

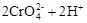 ,下列说法正确的是
,下列说法正确的是
| A.向该溶液中加入过量浓NaOH溶液后,溶液呈橙红色 |
| B.该反应不是氧化还原反应 |
| C.向该溶液中滴加适量的浓硫酸,平衡向逆反应方向移动,再次达到平衡后,氢离子浓度比原溶液大 |
D.该反应的平衡常数表达式是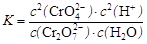 |
将一定量的氨基甲酸铵固体置于容积恒定的真空容器中,发生反应:H2NCOONH4(s)  2NH3(g)+CO2(g),在不同温度下,该反应达平衡状态时的部分数据如表所示。下列说法正确的是( )
2NH3(g)+CO2(g),在不同温度下,该反应达平衡状态时的部分数据如表所示。下列说法正确的是( )
| 温度 | 平衡浓度(mol·L-1) | |
| c(NH3) | c(CO2) | |
| T1 | 0.1 | |
| T2 | | 0.1 |
A.若T2>T1,则该反应的ΔH<0
B.向容器中充入N2,H2NCOONH4质量增加
C.NH3体积分数不变时,说明该反应达到平衡
D.T1、T2时,转化的H2NCOONH4的物质的量Δn(T2)=2Δn(T1)
下列各示意图与对应的表述正确的是 ( )
| A.图①表示一定条件下某化学反应的速率随时间变化的趋势图,该反应一定为放热反应 |
| B.图②中曲线表示将氢氧化钠溶液滴加到醋酸溶液浓度的变化趋势图 |
| C.图③表示等体积、等物质的量浓度的盐酸和醋酸溶液,分别加入足量镁粉,产生H2的物质的量的变化 |
| D.图④为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法 |
实验中要快速制取氢气,最好的方法是
| A.纯锌和稀硫酸反应 | B.纯锌和浓硫酸反应 |
| C.粗锌和浓硫酸反应 | D.粗锌与稀硫酸反应 |
认真研读课本是一种良好的学习习惯、按照课本所述,下列说法不正确的是( )
| A.护发素的主要功能是调节头发的pH,使之达到适宜的酸碱度 |
| B.厕所清洁剂、醋、肥皂、厨房清洁剂的pH依次增大 |
| C.仅用1mol/L KI溶液、0.1mol/L H2SO4溶液和淀粉溶液(仪器不限),就可以探究温度对化学反应速率的影响 |
| D.将少量Mg(OH)2沉淀和适量氯化铵溶液混合,无明显现象 |
在一定温度下,在固定容积的密闭容器中,可逆反应H2(g)+ Br2(g)  2HBr(g)达到平衡的标志是
2HBr(g)达到平衡的标志是
| A.断裂1 mol H-H键的同时生成2 mol H-Br键 |
| B.单位时间内消耗1 mol H2,同时生成1 mol Br2 |
| C.H2、Br2、HBr的分子数之比为1∶1∶2 |
| D.混合气体的压强不再改变 |