��Ŀ����
����Ŀ���Ҵ��������г��������ʣ���;�㷺����ϳɷ���������Ҳ�����о���ֵ��
I��ֱ���Ҵ�ȼ�ϵ����DEFC�����кܶ��ŵ㣬���������ǵ��о���Ȥ���������������Ҵ�ȼ�ϵ�ء�
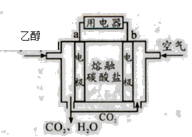
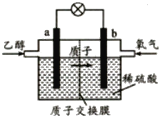
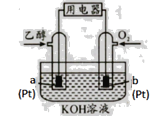
�����Ҵ�ȼ�ϵ�� �����Ҵ�ȼ�ϵ�� �������Ҵ�ȼ�ϵ��
��1�������Ҵ�ȼ�ϵ����������Ӧ���Ϊ____________��
��2�������Ҵ�ȼ�ϵ�������缫a�Ϸ����ĵ缫��ӦʽΪ________________________��ʹ�ÿ���������������ع��������м��Ի���½�����ԭ���� ____________��
��3�������Ҵ�ȼ�ϵ�������缫b�Ϸ����ĵ缫��ӦʽΪ_______________________��ͨ�����ӽ���Ĥ��������___________��
��4���������Ҵ�ȼ�ϵ������ѡ������̼���Ϊ���ʣ���ع���ʱ��CO32����缫____������a������b�����ƶ����缫b�Ϸ����ĵ缫��ӦʽΪ_____________________��
II����֪����ֱ��ˮ�Ϸ�������ȡ�Ҵ���H2O(g) + C2H4(g) ![]() CH3CH2OH(g)����n(H2O)�Un(C2H4)=1�U1ʱ����ϩ��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��
CH3CH2OH(g)����n(H2O)�Un(C2H4)=1�U1ʱ����ϩ��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��
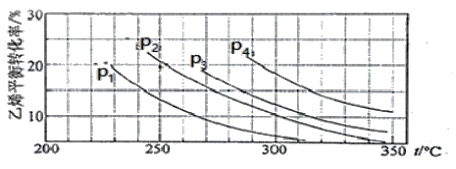
��1��ͼ��ѹǿP1��P2��P3��P4�Ĵ�С˳��Ϊ��_________________________�������ǣ�______________��
��2������ֱ��ˮ�Ϸ����õĹ�������Ϊ������/������Ϊ��������Ӧ�¶�290 ����ѹǿ6.9MPa��n(H2O)�Un(C2H4)=0.6�U1������������ϩ��ת����Ϊ5�G����Ҫ��һ�������ϩ��ת���ʣ����˿����ʵ��ı䷴Ӧ�¶Ⱥ�ѹǿ�⣬�����Բ�ȡ�Ĵ�ʩ��__________________________________��
���𰸡� ���� C2H5OH+16OH����12e��=CO32��+11H2O �����е�CO2����KOH��Һ��Ӧ��������Һ�ļ��ԣ�ͬʱ��Ӧ��Ҳ������KOH O2+12H+ +12e��6H2O H+ a O2+ 2CO2 +4e��=2CO32�� P4>P3>P2>P1 ��ӦΪ���������С�ķ�Ӧ������ѹǿƽ�������ƶ�����ϩ��ת��������������ͬ�����£�ת����Խ��Ĵ���ѹǿԽ�� ����H2O(g)�������Ƴ�������
���������� (1)ȼ�ϵ����ͨ��ȼ�ϵ�Ϊ������ͨ�������������Ϊ�����������Ҵ�ȼ�ϵ����������Ӧ���Ϊ������(2)�����Ҵ�ȼ�ϵ���У��缫aΪ�������缫��ӦʽΪC2H5OH+16OH����12e��=2CO32��+11H2O��ʹ�ÿ����������� �������е�CO2����KOH��Һ��Ӧ��������Һ�ļ��ԣ�ͬʱ��Ӧ��Ҳ������KOH���ʴ�Ϊ��C2H5OH+16OH����12e��=2CO32��+11H2O�������е�CO2����KOH��Һ��Ӧ��������Һ�ļ��ԣ�ͬʱ��Ӧ��Ҳ������KOH��(3)�����Ҵ�ȼ�ϵ���У��缫bΪ�������缫��ӦʽΪ3O2+12H+ +12e��= 6H2O��ͨ�����ӽ���Ĥ�ܹ�ʹ������H+��ͨ����(4)����ͼʾ��aΪ������ԭ��������������������ƶ���CO32����缫a�ƶ����缫bΪ�������缫��ӦʽΪO2+ 2CO2 +4e��= 2 CO32������ (1)����ͬ�¶���������ϩת����Ϊp1��p2��p3��p4����C2H4(g)+H2O(g)�TC2H5OH(g)��֪����ӦΪ���������С�ķ�Ӧ����������ѹǿ��ƽ�������ƶ�����ϩ��ת������ߣ����ѹǿ��ϵ��p1��p2��p3��p4���ʴ�Ϊ��p1��p2��p3��p4����ӦΪ���������С�ķ�Ӧ������ѹǿƽ�������ƶ�����ϩ��ת��������������ͬ�����£�ת����Խ��Ĵ���ѹǿԽ��(��)��Ҫ��һ�������ϩת���ʣ����˿����ʵ��ı䷴Ӧ�¶Ⱥ�ѹǿ�⣬�����Ըı����ʵ�Ũ�ȣ����ƽ����ϵ�н������Ҵ����������������ˮ������Ũ�ȣ��ı�������ʵ����ıȵȣ��ʴ�Ϊ���������Ҵ�Һ����ȥ������H2O(g)������

 �ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
�ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
