题目内容
【题目】根据反应Br+H2![]() HBr+H的能量随反应历程的变化示意图甲进行判断,下列叙述中不正确的是
HBr+H的能量随反应历程的变化示意图甲进行判断,下列叙述中不正确的是
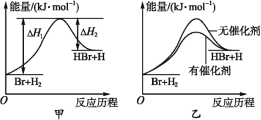
A. 正反应吸热
B. 加入催化剂,该化学反应的反应热不变
C. 加入催化剂后,该反应的能量随反应历程的变化示意图可用图乙表示
D. 加入催化剂可增大正反应速率,降低逆反应速率
【答案】D
【解析】
A、据反应物和生成物能量高低判断;
B、催化剂只能改变反应速率,不影响反应热;
C、催化剂通过降低反应的活化能改变反应历程;
D、催化剂能够同时降低正逆反应的活化能同等程度加快正逆反应速率。
A、反应物能量大于生成物,为吸热反应,选项A正确;
B、催化剂不能改变反应的反应热,选项B正确;
C、催化剂通过降低反应的活化能改变反应历程,选项C正确;
D、催化剂同时降低正、逆反应的活化能,同等程度加快正、逆反应速率,选项D错误;
答案选D。

【题目】温室效应是由于大气里温室气体(二氧化碳、甲烷等)含量增大而形成的。回答下列问题:
(1)利用CO2可以制取甲醇,有关化学反应如下:
①CO2(g)+3H2(g)CH3OH(g)+H2O(g ) ΔH1=-178 kJ/mol
②2CO(g)+O2(g)2CO2(g) ΔH2=-566 kJ/mol
③2H2(g)+O2(g)2H2O(g) ΔH3=-483.6 kJ/mol
已知反应①中相关的化学键键能数据如下:
化学键 | C—C | C—H | H—H | C—O | H—O |
键能/ kJ/mol | 348 | 413 | 436 | 358 | 463 |
由此计算断开1 mol C![]() O需要吸收____________kJ的能量(甲醇的球棍模型如图所示
O需要吸收____________kJ的能量(甲醇的球棍模型如图所示 );
);
CO(g)+2H2(g)CH3OH(g) ΔH=________ kJ/mol。
(2)甲烷燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC工作原理如下图所示:通入a气体的电极是原电池的______极(填“正”或“负”),其电极反应式为___________________。

(3)下图是用甲烷燃料电池(电解质溶液为KOH溶液)实现铁上镀铜,则b处通入的是______(填“CH4”或“O2”),电解前,U形管的铜电极、铁电极的质量相等,电解2min后,取出铜电极、铁电极,洗净、烘干、称量,质量差为12.8g,在通电过程中,电路中通过的电子为_____mol,消耗标准状况下CH4________mL。