题目内容
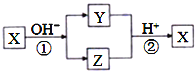
【题目】X是中学化学常见的单质,Y、Z为化合物。它们有如图所示的转化关系(部分产物及反应条件省略)。下列判断正确的是
A. X可能是金属,也可能是非金属
B. X、Y、Z含有一种相同的元素
C. Y、Z的水溶液一定都呈碱性
D. 反应①②不一定都是氧化还原反应
【答案】B
【解析】
单质X与强碱反应生成Y和Z两种物质,则X可能为卤素单质、金属铝或硅单质等,Y和Z能在酸性条件下反应生成X,则X可能为S单质或卤素单质Cl2、Br2等。据此分析。
单质X与强碱反应生成Y和Z两种物质,则X可能为卤素单质、金属铝或硅单质等,Y和Z能在酸性条件下反应生成X,则X可能为S单质或卤素单质Cl2、Br2等。
A项,根据上述分析,X只能是卤素单质即非金属单质,故A项错误;
B项,X遇强碱发生歧化反应,生成Y和Z,则X、Y、Z中含相同的元素,故B项正确;
C项,X以Cl2为例,Y、Z的阴离子可能为Cl-或ClO-,若阴离子为Cl-,则溶液呈中性,若阴离子为ClO-,则溶液呈碱性,故C项错误;
D项,根据分析,反应①中单质X发生歧化反应生成Y和Z,反应②中Y和Z发生归中反应生成X,二者均为氧化还原反应,故D项错误。
综上所述,本题正确答案为B。

练习册系列答案
相关题目
【题目】短周期元素X、Y、Z在元素周期表中的位置如图所示,回答下列问题。
X | ||
Y | ||
Z |
(1)元素X的单质分子是____(写化学式)。
(2)Y位于元素周期表中的第____周期,第_____族。
(3)比Z原子序数大的同主族且相邻周期的元素的原子序数是______。