题目内容
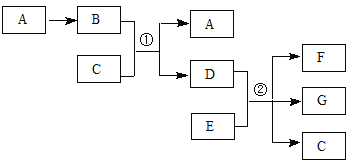
【题目】空气吹出法工艺是目前“海水提溴”的最主要方法之一。其工艺流程如下:
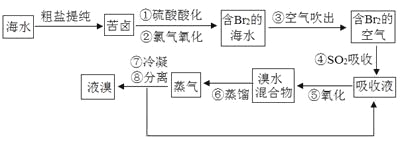
(1)步骤①中氯气氧化溴离子时在pH=3.5的酸性条件下效果最好,当使用精确pH试纸(能读数到0.1)检测步骤②氯气氧化的溶液的pH时,发现其颜色变化失常,则pH检测失败的原因是 。
(2)步骤④中反应的化学方程式为 ,该反应中体现了SO2的 性(填“氧化”或“还原”)。
(3)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,在实验室可用分液漏斗进行分离。分离时从分液漏斗的上口倒出的是 。
(4)步骤①、②之后并未直接用“含Br2的海水”进行蒸馏得到液溴,而是经过“空气吹出”、“SO2吸收”、“氧化”后再蒸馏,“空气吹出、SO2吸收、氧化”的过程实际上是一个Br2的 过程,与直接蒸馏含Br2的海水相比优点是消耗更少成本降低和
【答案】(1) 溶液中的HClO将pH试纸漂白 ;(2) SO2 + Br2 + 2H2O = H2SO4+ 2HBr,还原; (3)溴水;(4) 浓缩(或富集),效率更高。
【解析】试题分析:空气吹出法是用于工业规模海水提溴的常用方法,其中一种工艺是在预先经过酸化的浓缩海水中,用氯气置换溴离子使之成为单质溴,继而通入空气和水蒸气,将溴吹入吸收塔,使溴蒸汽和吸收剂二氧化硫发生作用转化成氢溴酸以达到富集的目的,也就是得到富集溴.然后,再用氯气将其氧化得到产品溴。(1)步骤①中氯气氧化溴离子时在pH=3.5的酸性条件下效果最好,当使用精确pH试纸(能读数到0.1)检测步骤②氯气氧化的溶液的pH时,发现其颜色变化失常,则pH检测失败的原因是,溶液中的HClO将pH试纸漂白;(2)Br2和SO2发生氧化还原反应生成HBr和H2SO4,反应的方程化学方程式为:Br2+SO2+2H2O=H2SO4+2HBr,反应中二氧化硫中硫元素化合价+4价升高到+6价,体现二氧化硫的还原性;(3)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,在实验室可用分液漏斗进行分离,液溴密度大于水,分离时从分液漏斗的上口倒出的是溴水;(4)氯化后的海水虽然含有溴单质,但浓度低,产量低,应经过“空气吹出、SO2吸收、氯化”的过程进行富集,如果直接蒸馏原料,产品成本高,与直接蒸馏含Br2的海水相比优点是消耗更少成本,效率更高,故与直接蒸馏含Br2的海水相比优点是消耗更少成本降低和效率更高。

 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案