题目内容
锌—空气电池可能成为未来的理想动力源,该电池的电解质溶液可以是酸性或碱性。在碱性溶液中该电池总反应可表示为:2Zn+4NaOH+O2=2Na2ZnO2 +2H2O。下列有关锌-空气电池说法正确的是
| A.碱性电解质溶液中正极反应式为:4OH-- 4e-= O2↑+2H2O |
| B.碱性或酸性电解质溶液中,该电池正极反应式相同 |
| C.该电池工作时,Na+移向负极 |
| D.每生成1 mol ZnO22-转移电子数为2NA |
D
解析试题分析:A、碱性电解质溶液中正极应为O2得电子,错误;B、酸性溶液中正极反应式为:O2+4H++4e?=2H2O,碱性溶液中正极反应式为:O2+H2O+4e?=4OH?,正极反应式不同,错误;C、该电池工作时,Na+移向正极,错误;D、Zn元素化合价由0价升高至+2价,所以每生成1 mol ZnO22-转移电子数为2NA,正确。
考点:本题考查原电池原理及应用。

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
某小组为研究电化学原理,设计如图装置。下列叙述错误的是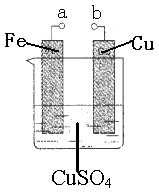
| A.a和b不连接时,铁片质量会增加 |
| B.a和b用导线连接时,正极发生的电极反应为:Cu2++2e-=Cu |
| C.无论a和b是否连接,铁片均被腐蚀 |
| D.a和b分别连接电源正、负极时,Fe电极发生的电极反应为:4OH--4e-=2H2O+O2↑ |
下列叙述中错误的是
| A.电解池是电能转化为化学能的装置 |
| B.原电池跟电解池链接后,电子从原电池负极流向电解池阳极 |
| C.电镀时,电镀池里的阳极材料发生氧化反应 |
| D.用惰性电极电解饱和食盐水时,阴极得到氢氧化钠溶液和氢气 |
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。其反应原理如下:电池 Pb(s) + PbO2(s) + 2H2SO4(aq) =2PbSO4(s) + 2H2O(l)
电解池 2Al + 3H2O = Al2O3 + 3H2,对该电解过程,以下判断正确的是
| | 电池 | 电解池 |
| A | H+移向Pb电极 | H+移向Pb电极 |
| B | 每消耗3molPb | 生成1molAl2O3 |
| C | 正极:PbO2+4H++2e—=Pb2++2H2O | 阳极:2Al+3H2O—6e—=Al2O3+6H+ |
| D | Pb电极反应质量不变 | Pb电极反应质量不变 |
下列有关用惰性电极电解AgNO3溶液的说法不正确的是:
| A.电解过程中阴极质量不断增大 |
| B.电解过程中阳极附近的pH不断降低 |
| C.电解一段时间后,向溶液中加入适量的Ag2O固体可使溶液恢复到电解前的状况 |
| D.电解过程中,溶液中电子由阴极迁向阳极 |
不能用Fe+H2SO4=FeSO4+H2↑表示的是( )
| A.用导线将铁片和铜片连接后,放入一盛有稀 H2SO4溶液的烧杯中 |
| B.将铁片直接放入一盛有稀 H2SO4溶液的烧杯中 |
| C.Cu片作阳极,铁片作阴极,电解一定量的H2SO4溶液 |
| D.Cu片作阴极,铁片作阳极,电解一定量的H2SO4溶液 |
下列与金属腐蚀有关的说法正确的是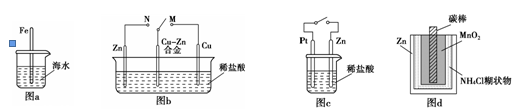
| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,开关由M改置于N时,Cu?Zn合金的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
| D.图d中,Zn-MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的 |
下列说法中正确的是
| A.在船体上镶嵌锌块,可以减缓船体被海水腐蚀的速率 |
| B.粗铜精炼时,电镀液中的c(Cu2+)保持不变 |
| C.纯银在空气中久置变黑发生的是电化学腐蚀 |
| D.阴极电保护法是将被保护的金属与外加电源的正极相连 |
“天宫一号”飞行器白天靠太阳能帆板产生电流向镍氢电池充电,夜间镍氢电池向飞行器供电。镍氢电池结构示意图如图。若电池总反应为:Ni(OH)2  NiOOH+1/2H2,充电时阴极反应为:H2O+e-=1/2H2+OH-。则下列说法正确的是( )
NiOOH+1/2H2,充电时阴极反应为:H2O+e-=1/2H2+OH-。则下列说法正确的是( )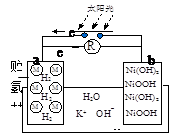
| A.充电时a极为正极 |
| B.放电时NiOOH发生氧化反应 |
| C.充电时,OH-向移a极, K+移向b极 |
| D.放电时正极反应为:NiOOH + H2O +e- = Ni(OH)2 + OH- |