题目内容
【题目】某温度下,反应:2A(g)B(g)+C(g)的平衡常数为1,在容积为2L的密闭容器中加入A(g),20s时测得各组分的物质的量如下表:下列说法正确的是( )
物质 | A(g) | B(g) | C(g) |
物质的量/mol | 1.2 | 0.6 | 0.6 |
A.反应前20 s内的平均反应速率为v(A)=0.6 molL﹣1s﹣1
B.20 s时,正反应速率大于逆反应速率
C.达到平衡时,A(g)的转化率为100%
D.若升高温度平衡常数变为2,则反应的△H<0
【答案】B
【解析】解:A、反应前只有反应物A,所以反应前20 s内物质A消耗0.6×2=1.2 mol,v(A)= ![]() =0.03 molL﹣1s﹣1 , 故A错误;
=0.03 molL﹣1s﹣1 , 故A错误;
B、20 s时,Q= 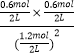 =0.25,比K小,尚未达到平衡,故B正确;
=0.25,比K小,尚未达到平衡,故B正确;
C、可逆反应不可能完全转化,故C错误;
D、升高温度,平衡常数增大,平衡向正反应方向进行,则正反应吸热,故D错误.
故选:B.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目