题目内容
A、B、C、D四种非金属元素,A、B在反应中各结合1个电子形成稳定结构,放出能量B<A,氢化物稳定性HD>HA,原子序数C<B,其稳定结构的核外电子数相等,则四种元素非金属性由强到弱的顺序正确的是A.A、B、C、D B.B、A、C、D C.D、A、B、C D.B、A、D、C
C
解析:非金属原子结合同数量的电子形成稳定结构,放出能量多的,元素的非金属性越强,放出能量B<A,则非金属性A>B。气态氢化物越稳定,元素的非金属性越强,气态氢化物的稳定性HD>HA,则元素的非金属性D>A。由原子序数C<B,其稳定结构的核外电子数相等,说明C、B处在同一周期,同周期元素自左向右,元素的非金属性增强,则元素的非金属性B>C。

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
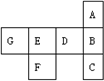 (2010?卢湾区二模)“椅子形状”的图包含了元素周期表前四周期的部分元素,其中A、B、C、D四种元素原子序数之和为77.
(2010?卢湾区二模)“椅子形状”的图包含了元素周期表前四周期的部分元素,其中A、B、C、D四种元素原子序数之和为77.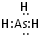
 ”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“ ”表示氢原子,小黑点“
”表示氢原子,小黑点“


 ,判断其中的化学键的类型
,判断其中的化学键的类型