题目内容
某化学小组在学习元素周期律知识后,对教材中Cl2将Fe2+氧化成Fe3+的实验进一步思考,并提出问题:Cl2能将Fe2+氧化成Fe3+,那么Br2和I2能否将Fe2+氧化成Fe3+?
环节一:理论推测。
部分同学认为Br2和I2都能将Fe2+氧化成Fe3+,依据是____________________
_________________________________________________________________。
部分同学认为Br2和I2都不能将Fe2+氧化成Fe3+。还有同学认为Br2能将
Fe2+氧化成Fe3+,而I2不能,依据是同一主族从上到下卤素单质的氧化性逐渐减弱。
环节二:设计实验进行验证。
向大试管中加入适量铁粉,加入10 mL稀盐酸,振荡试管,充分反应后,铁粉有剩余,取上层清液进行下列实验。
实验1:
试管 | 操作 | 现象 |
① | 先向试管中加入2 mL新制的FeCl2溶液,再向试管中滴加少量红棕色的溴水,振荡试管 | 溶液为 黄色 |
② | 先向试管中加入2 mL新制的FeCl2溶液,再向试管中滴加少量棕黄色的碘水,振荡试管 | 溶液为 黄色 |
环节三:实验现象的分析与解释。
(1)甲同学认为试管①中的现象说明溴水能将Fe2+氧化,反应的离子方程式为_________________________________________________________________。
乙同学认为应该补做实验,才能得出甲同学的结论。请你帮助乙同学完成实验:
实验2:
操作 | 现象 |
|
|
(2)该小组同学对试管②中所得的溶液呈黄色的原因展开讨论,并提出了两种假设:
假设1:碘水与FeCl2溶液不反应,黄色是碘水稀释后的颜色。
假设2.________________。
实验3:进行实验以判断假设是否成立。
操作 | 现象 |
向试管②所得的溶液中继续加入0.5 mL CCl4,充分振荡,静置一段时间。取出上层溶液,滴加KSCN溶液 | 静置后,上层溶液几乎无色,下层溶液为紫色;取上层溶液滴加KSCN溶液后,溶液呈浅红色 |
丙同学认为实验3的现象可以说明假设2成立,丁同学认为不严谨,于是设计了实验4继续探究。
实验4:
操作 | 现象 |
向另一支试管中加入2 mL新制的FeCl2溶液,滴加0.5 mL碘水后,再加入0.5 mL乙酸乙酯,充分振荡,静置一段时间。取出下层溶液,滴加KSCN溶液 | 静置后,上层溶液为紫色,下层溶液几乎无色;取下层溶液,向其中滴加KSCN溶液后,溶液没有呈浅红色 |
你认为实验4中加入乙酸乙酯的主要目的是___________________________。
丁同学根据实验4的现象得出结论:在本次实验条件下,碘水与FeCl2溶液反应的程度很小。
(3)Cl2、Br2、I2氧化Fe2+的能力逐渐减弱,从原子结构角度解释原因:______________________________________________________________________。
环节一:均为ⅦA族元素,其单质的氧化性均较强环节三:(1)2Fe2++Br2=2Fe3++2Br-
操作 | 现象 |
取少量试管①中的黄色溶液于试管③中,滴加少量KSCN溶液,振荡 | 溶液变为红色 |
(2)碘水与FeCl2溶液发生反应,FeCl3溶液呈黄色 亚铁离子与空气接触会被氧化,加入的乙酸乙酯既可作萃取剂又能起到液封的作用,防止空气对实验产生干扰
(3)同一主族元素从上到下,原子核外的电子层数依次增多,原子半径逐渐增大,得电子能力逐渐减弱,氧化性逐渐减弱
【解析】由题给信息和实验目的可知部分同学认为Br2和I2都能将Fe2+氧化成Fe3+的依据是这些单质均为ⅦA族元素的单质,氧化性均较强。
(1)实验1的试管①中发生反应的离子方程式为2Fe2++Br2=2Fe3++2Br-。由于甲同学的结论仅仅是根据溶液颜色的变化得出的,所以结论不一定可靠,必须通过实验进行验证,可探究该过程中是否有三价铁离子生成,所以实验的设计应是三价铁离子的检验,故对应的方案为取少量试管①中的黄色溶液于试管③中,滴加少量KSCN溶液,振荡,若溶液变为红色则表明有三价铁离子生成。
(2)可根据物质的颜色分析试管②中所得溶液呈黄色的可能原因,一是碘水的颜色,二是三价铁离子的颜色。实验方案的设计需从这两个方面进行考虑,同时需要考虑亚铁离子在空气中容易被氧化成三价铁离子,所以实验的设计必须排除空气的影响,即实验4中加入乙酸乙酯的主要目的一是乙酸乙酯可作萃取剂,二是防止空气中的氧气将亚铁离子氧化成三价铁离子。

 名校课堂系列答案
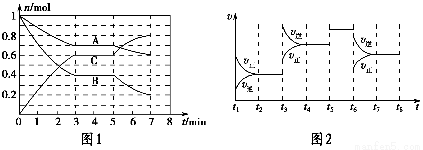
名校课堂系列答案25 ℃时,在体积为2 L的密闭容器中,气态A、B、C的物质的量n随时间t的变化如图1所示,已知达到平衡后,降低温度,A的转化率将增大。
t2~t3 | t4~t5 | t5~t6 | t7~t8 |
K1 | K2 | K3 | K4 |
(1)根据图1数据,写出该反应的化学方程式:__________________。此反应的平衡常数表达式K=________,从反应开始到第一次平衡时的平均速率v(A)为________。
(2)在5~7 min内,若K值不变,则此处曲线变化的原因是________________。
(3)如图2表示此反应的反应速率v和时间t的关系图,各阶段的平衡常数如表所示。K1、K2、K3、K4之间的关系为________(用“>”、“<”或“=”连接)。A的转化率最大的一段时间是________。