题目内容
7.下列关于化学反应与能量的说法不正确的是( )| A. | 在化学反应中,断开化学键要吸收能量,形成化学键要放出能量 | |
| B. | 化学反应除了生成新物质外,还伴随着能量的变化 | |
| C. | 若反应物的总能量高于生成物的总能量,则该反应必为吸热反应 | |
| D. | 铝热反应是放热反应 |
分析 A.断键吸收能量,成键放出能量;
B.能量变化是化学反应的基本特征,物质发生化学反应都是伴随着能量的变化;
C.在一个确定的化学反应关系中,反应物的总能量既可以高于生成物的总能量又可以低于生成物的总能量;
D.铝热反应的特征为放出大量的热.
解答 解:A.断键吸收能量,成键放出能量,化学变化中的能量变化主要是由化学键变化引起的是对的,故A正确;
B.化学变化中的能量变化主要是由化学键变化引起的是对的,物质发生化学反应都是伴随着能量的变化,能量变化是化学反应的基本特征,故B正确;
C.反应物的总能量既可以高于生成物的总能量又可以低于生成物的总能量,若反应物的总能量高于生成物的总能量,则该反应必为放热反应,故C错误;
D.铝热反应的特征为放出大量的热,所以铝热反应是放热反应,故D正确.故选C.
点评 本题是对化学变化与能量的考查,解决的关键是明确化学变化的实质与化学键的关系,属基础性知识考查题.

练习册系列答案
相关题目
17.某实验小组用工业上废渣(主要成分Cu2S和Fe2O3)制取纯铜和绿矾(FeSO4•7H2O)产品,设计流程如下:

(1)在实验室中,欲用98%的浓硫酸(密度为1.84g•mL-1)配制500mL1.0mol•L-1的硫酸,需要的仪器除量筒、烧杯、玻璃棒外,还有胶头滴管、500mL容量瓶.
(2)该小组同学设计如下装置模拟废渣在过量氧气中焙烧,并验证废渣中含硫元素.
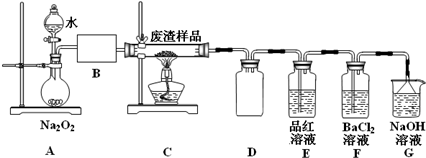
①装置A中反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑;为控制反应不过于激烈并产生平稳气流,采取的操作及现象是打开分液漏斗上口活塞,控制分液漏斗旋塞,使水匀速逐滴滴下;B处应连接盛有碱石灰的干燥管(或U形管)或浓硫酸的洗气瓶(填写试剂及仪器名称).
②E装置中加入品红溶液的目的是检验气体a中的SO2;当F装置中出现白色沉淀时,反应离子方程式为2SO2+O2+2H2O+2Ba2+=2BaSO4↓+4H+.
(3)下列操作中,不属于步骤⑤中进行的操作的是ad(填下列各项中序号).
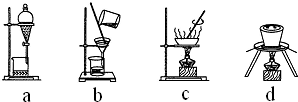
步骤⑥中由粗铜得到纯铜的方法为电解精炼(填写名称).
(4)为测定产品中绿矾的质量分数,称取30.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,反应为:10FeSO4+8H2SO4+2KMnO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O.实验所得数据如下表所示:
①第1组实验数据出现异常,造成这种异常的原因可能是ad(填代号).
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时俯视读数
d.滴定终点时仰视读数
②根据表中数据,计算所得产品中绿矾的质量分数为92.7%.

(1)在实验室中,欲用98%的浓硫酸(密度为1.84g•mL-1)配制500mL1.0mol•L-1的硫酸,需要的仪器除量筒、烧杯、玻璃棒外,还有胶头滴管、500mL容量瓶.
(2)该小组同学设计如下装置模拟废渣在过量氧气中焙烧,并验证废渣中含硫元素.

①装置A中反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑;为控制反应不过于激烈并产生平稳气流,采取的操作及现象是打开分液漏斗上口活塞,控制分液漏斗旋塞,使水匀速逐滴滴下;B处应连接盛有碱石灰的干燥管(或U形管)或浓硫酸的洗气瓶(填写试剂及仪器名称).
②E装置中加入品红溶液的目的是检验气体a中的SO2;当F装置中出现白色沉淀时,反应离子方程式为2SO2+O2+2H2O+2Ba2+=2BaSO4↓+4H+.
(3)下列操作中,不属于步骤⑤中进行的操作的是ad(填下列各项中序号).

步骤⑥中由粗铜得到纯铜的方法为电解精炼(填写名称).
(4)为测定产品中绿矾的质量分数,称取30.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,反应为:10FeSO4+8H2SO4+2KMnO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O.实验所得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.90 | 20.02 | 19.98 | 20.00 |
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时俯视读数
d.滴定终点时仰视读数
②根据表中数据,计算所得产品中绿矾的质量分数为92.7%.
18.25℃时,0.1mol•L-1氨水中$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-8,下列叙述正确的是( )
| A. | 该溶液中氢离子的浓度:c(H+)=1×10-11mol•L | |
| B. | pH=7的NH4Cl和NH3•H2O的混合溶液:c(Cl-)>c(NH4+)>c(H+)>c(H+)=c(OH-) | |
| C. | 浓度均为0.1mol•L-1的NH3•H2O和NH4Cl溶液等体积混合后的碱性溶液中:c(NH4+)>c(Cl-)>c(NH3•H2O)>c(OH-)>c(H+) | |
| D. | 0.1mol•L-1的氨水与0.05mol的H2SO4溶液等体积混合后所得溶液中:2c(NH4+)+2c(NH3•H2O)=c(SO42-) |
15.下列元素不属于长周期元素的是( )
| A. | Cs | B. | Cl | C. | Fe | D. | Br |
2.下列说法正确的是( )
| A. | 可用苯萃取四氯化碳中的碘 | |
| B. | 苯滴入溴水中,发生取代反应生成溴苯 | |
| C. | 可用石蕊溶液区分乙醇和乙酸两种物质 | |
| D. | 等物质的量的甲烷与氯气混合光照至充分反应,产物中最多的是四氯化碳 |
12.下列实验操作、现象、结论均正确的是( )
| 实验操作 | 现象 | 结论 | |
| A | 淀粉溶液中加入碘水 | 溶液变蓝 | 说明淀粉没有水解 |
| B | 将乙醇与酸性重铬酸钾(K2Cr2O7)溶液混合 | 橙色溶液变为绿色 | 乙醇具有还原性 |
| C | 向某未知溶液中加入BaCl2溶液后,再加入稀硝酸观察 | 沉淀的生成 | 检验是否含SO42- |
| D | 向某未知溶液中加入NaOH浓溶液,加热,在试管口用湿润的蓝色石蕊试纸检验 | 试纸变红 | 检验是否含NH4+ |
| A. | A | B. | B | C. | C | D. | D |
19.下列有关说法正确的是( )
| A. | 1 mol Cl2参加反应转移电子数一定为2NA | |
| B. | 在反应KIO3+6HI═KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA | |
| C. | Na2O2与CO2反应生成标况下11.2L O2,反应过程中转移电子数1 NA | |
| D. | 反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4该反应FeS2中的硫元素全部被氧化 |
16.有M、X、Y、Z、W五种原子序数依次增大的短周期元素,其中M、Z同主族; X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料.下列说法正确的是( )
| A. | X、M两种元素形成的化合物只能存在离子键 | |
| B. | 元素Y、Z、W的单质晶体属于同种类型的晶体 | |
| C. | 由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低 | |
| D. | 元素W和M的某些单质可作为水处理中的消毒剂 |
17.下列反应的离子方程式正确的是( )
| A. | 碳酸氢镁溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+MgCO3↓ | |
| B. | 1mo•L-1 的 NaAlO2 溶液和2.5mol•L-1 的盐酸等体积混合:2AlO2-+5 H+=Al(OH)3↓+Al3++H2 O | |
| C. | 亚硫酸氢钡溶液中加入适量双氧水:HSO3-+H2O2=SO42-+H2O+H+ | |
| D. | 硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:Fe2++2H++H2O2=Fe3++2H2O |